
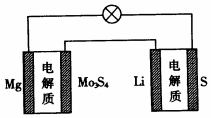
 已知:鎂電池的總反應為xMg+Mo3S4$?_{放電}^{充電}$MgxMo3S4,鋰硫電池的總反應為2Li+S$?_{放電}^{充電}$Li2S.下列說法正確的是( )
已知:鎂電池的總反應為xMg+Mo3S4$?_{放電}^{充電}$MgxMo3S4,鋰硫電池的總反應為2Li+S$?_{放電}^{充電}$Li2S.下列說法正確的是( )| A. | 鎂電池放電時,Mg2+向負極遷移 | |
| B. | 鎂電池放電時,正極發生的電極反應為Mo3S4+2xe-=Mo3S42- | |
| C. | 理論上兩種電池的比能量相同(參與電極反應的單位質量的電極材料放出電能的大小稱為該電池的比能量) | |
| D. | 圖中Li作負極,Mo3S4作陽極 |
分析 A.原電池中陽離子向正極移動;
B.原電池中正極發生還原反應,得電子化合價降低;
C.比能量是參與電極反應的單位質量的電極材料放出電能的大小;
D.多池相連,含活潑強的電極為原電池,其它電池為電解池.
解答 解:A.原電池中陽離子向正極移動,則鎂電池放電時,Mg2+向正極遷移,故A錯誤;
B.原電池中正極發生還原反應,得電子化合價降低,所以正極發生的電極反應為Mo3S4+2xe-=Mo3S42-,故B正確;
C.比能量是參與電極反應的單位質量的電極材料放出電能的大小,鋰硫電池放電時負極為Li,鎂電池放電時負極為鎂,兩種電池的負極材料不同,所以比能量不同,故C錯誤;
D.多池相連,含活潑強的電極為原電池,其它電池為電解池,活潑強的是鋰,所以右邊是原電池,左邊是電解池,鋰是負極,與之相連的Mo3S4作陰極,故D錯誤;
故選B.
點評 本題考查了二次電池,為高頻考點,側重于對原電池原理和電解池原理的考查,題目難度中等,注意根據電池總反應判斷正負極材料及電極反應.


科目:高中化學 來源: 題型:選擇題
| A. | Si與SiO2在常溫下都可與NaOH溶液反應 | |
| B. | C與SiO2之間可以反應制備Si,同時得到CO | |
| C. | Si與SiO2都可以與氫氟酸反應 | |
| D. | Si→SiO2→H2SiO3可以通過一步反應實現 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
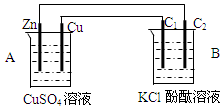 按圖裝置進行實驗,并回答下列問題
按圖裝置進行實驗,并回答下列問題查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
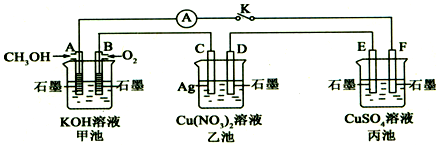
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
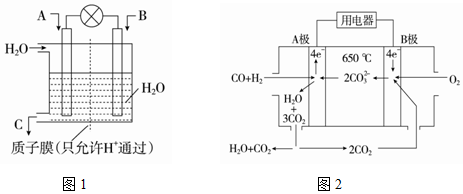
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 物質 | 顏色 | 水中溶解性 |
| Fe2S3 | 黑色 | 難溶于水 |
| FeS | 黑褐色 | 難溶于水 |
| 實驗步驟 | 操作 | 現象 | 備注 |
| 1 | 向2mL 0.1mol/L氯化鐵溶液中逐滴滴入3滴0.1mol/L 硫化鈉溶液 | 產生黑色沉淀,立即變為黃色沉淀,未見其它明顯現象 | 自始至終都未見紅褐色沉淀 |
| 2 | 繼續滴加3滴0.1mol/L 硫化鈉溶液 | 同上 | |
| 3 | 繼續滴加0.1mol/L 硫化鈉溶液至過量 | 產生黑色沉淀,振蕩后靜置,未發現明顯變化 |
| 實驗步驟 | 操作 | 現象 |
| 4 | 向2mL 0.1mol/L硫化鈉溶液中逐滴滴入3滴0.1mol/L 氯化鐵溶液 | 產生黑色沉淀,未見其它明顯現象 |
| 5 | 繼續滴加3滴0.1mol/L 氯化鐵溶液 | 同上 |
| 6 | 繼續滴加0.1mol/L 氯化鐵溶液至過量 | 同上 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
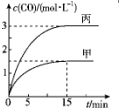 一定條件下存在反應C(s)+H2O(g)?CO(g)+H2(g)△H>0.向甲、丙兩個恒容容器中加入一定量C和H2O(g),向乙恒容容器中加入一定量CO和H2,各容器中溫度、反應物的起始量如表,甲、丙反應過程中CO的物質的量濃度隨時間變化如圖.
一定條件下存在反應C(s)+H2O(g)?CO(g)+H2(g)△H>0.向甲、丙兩個恒容容器中加入一定量C和H2O(g),向乙恒容容器中加入一定量CO和H2,各容器中溫度、反應物的起始量如表,甲、丙反應過程中CO的物質的量濃度隨時間變化如圖.| 容器 | 甲 | 乙 | 丙 |
| 容積 | 0.5L | 0.5L | V |
| 溫度 | T1℃ | T2℃ | T1℃ |
| 起始量 | 2mol C、 1mol H2O(g) | 1mol CO、 1mol H2 | 4mol C、 2mol H2O(g) |
| A. | 丙容器的容積V<0.5L | |
| B. | 甲容器中,反應在前15 min內的平均反應速率v(H2)=0.15 mol•L-1•min-1 | |
| C. | 當溫度為T1℃時,反應的平衡常數K=2.25 | |
| D. | 乙容器中,若平衡時n(H2O)=0.3 mol,則T1<T2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 煤、石油、天然氣屬于化石能源,太陽能、氫能、風能、地熱能、海洋能屬于新能源 | |
| B. | 白鐵(鍍鋅鐵板)比馬口鐵(鍍錫鐵板)更耐腐蝕 | |
| C. | 為防止電池中的重金屬等污染土壤和水體,應采取深度填埋法 | |
| D. | 測試和調控溶液的pH對工農業生產、科學研究及日常生活和醫療保健都有重要意義 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com