
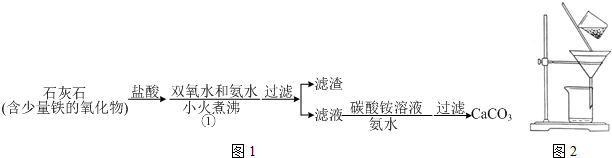
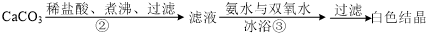
分析 (一)碳酸鈣的制備
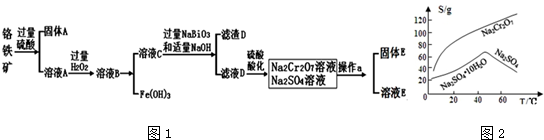
由流程可知,加鹽酸,碳酸鈣、鐵的氧化物均溶解,加雙氧水可氧化亞鐵離子,加氨水將鐵離子轉化為沉淀,過濾后的濾液中含鹽酸,加氨水中和酸,利用得到碳酸鈣沉淀;
(1)堿可中和酸,小火煮沸利于沉淀生成;
(2)過濾遵循一貼二低三靠;
(二)過氧化鈣的制備
由流程可知,碳酸鈣溶于鹽酸后,至溶液中尚存有少量固體,過濾后,濾液中氯化鈣、氨水、過氧化氫反應生成CaO2、NH4Cl、水;再過濾,洗滌得到過氧化鈣;制備過氧化鈣的另一種方法是:將石灰石煅燒后,直接加入雙氧水反應,過濾后可得到過氧化鈣產品,石灰石便宜易得,但純度較低,以此來解答.
解答 解:(一)碳酸鈣的制備
由流程可知,加鹽酸,碳酸鈣、鐵的氧化物均溶解,加雙氧水可氧化亞鐵離子,加氨水將鐵離子轉化為沉淀,過濾后的濾液中含鹽酸,加氨水中和酸,利用得到碳酸鈣沉淀;
(1)步驟①加入氨水的目的是中和多余的鹽酸,沉淀鐵離子.小火煮沸的作用是使沉淀顆粒長大,有利于過濾,
故答案為:調節溶液pH使Fe(OH)3沉淀;過濾分離;
(2)a.漏斗末端頸尖未緊靠燒杯壁,應漏斗末端頸尖緊靠燒杯壁,故錯誤;
b.玻璃棒用作引流,使液體順利流下,故正確;
c.將濾紙濕潤,使其緊貼漏斗壁,防止液體從濾紙與漏斗的縫隙流下,故正確;
d.濾紙邊緣應低于漏斗上邊緣,故錯誤;
e.玻璃棒不能在漏斗中輕輕攪動以加過過濾速度,可能搗破濾紙,過濾失敗,故錯誤;
故答案為:ade;
(二)過氧化鈣的制備
由流程可知,碳酸鈣溶于鹽酸后,至溶液中尚存有少量固體,過濾后,濾液中氯化鈣、氨水、過氧化氫反應生成CaO2、NH4Cl、水;再過濾,洗滌得到過氧化鈣;
(3)步驟②的具體操作為逐滴加入稀鹽酸,至溶液中尚存有少量固體,溶液中溶解二氧化碳,此時溶液呈酸性;將溶液煮沸,趁熱過濾,將溶液煮沸的作用是除去溶液中溶解的二氧化碳,
故答案為:酸;除去溶液中溶解的二氧化碳;
(4)步驟③中反應的化學方程式為CaCl2+2NH3.H2O+H2O2=CaO2+2NH4Cl+2H2O,該反應需要在冰浴下進行,原因是溫度過高時雙氧水易分解,
故答案為:CaCl2+2NH3.H2O+H2O2+6H2O=CaO2•8H2O↓+2NH4Cl;溫度過高時雙氧水易分解;
(5)將過濾得到的白色結晶依次使用蒸餾水、乙醇洗滌,使用乙醇洗滌的目的是去除晶體表面水分,
故答案為:去除晶體表面水分;
(6)制備過氧化鈣的另一種方法是:將石灰石煅燒后,直接加入雙氧水反應,過濾后可得到過氧化鈣產品.該工藝方法的優點是原料來源豐富、操作簡單,產品的缺點是純度較低,
故答案為:工藝簡單、操作方便;純度較低.
點評 本題考查物質的制備實驗,為高頻考點,把握制備實驗原理、實驗技能、物質的性質為解答的關鍵,側重分析與實驗能力的考查,注意物質的性質及應用,題目難度中等.


 優等生題庫系列答案
優等生題庫系列答案 53天天練系列答案
53天天練系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
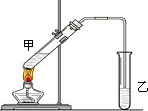 俗話說,“陳酒老醋特別香”,其原因是酒在儲存過程中生成了有香味的乙酸乙酯,在實驗室里我們也可以用如圖所示的裝置來模擬該過程.請回答下列問題:
俗話說,“陳酒老醋特別香”,其原因是酒在儲存過程中生成了有香味的乙酸乙酯,在實驗室里我們也可以用如圖所示的裝置來模擬該過程.請回答下列問題: .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
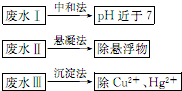 水處理技術在生產、生活中應用廣泛,對工業廢水和生活污水進行處理是防止水體污染、改善水質的主要措施.
水處理技術在生產、生活中應用廣泛,對工業廢水和生活污水進行處理是防止水體污染、改善水質的主要措施.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
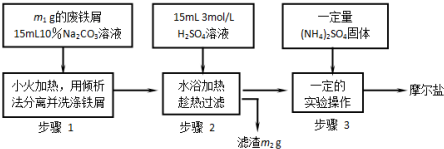
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
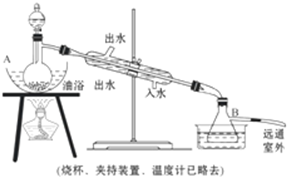
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
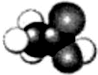 乙酸是食醋的主要成分,它的分子結構模型如圖所示.
乙酸是食醋的主要成分,它的分子結構模型如圖所示.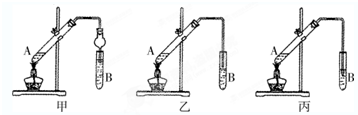
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com