
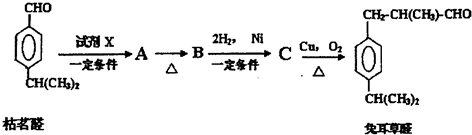
 ;檢驗B中的官能團時,需先加入的試劑是新制氫氧化銅懸濁液;酸化后,再加入的試劑是溴水或高錳酸鉀溶液.
;檢驗B中的官能團時,需先加入的試劑是新制氫氧化銅懸濁液;酸化后,再加入的試劑是溴水或高錳酸鉀溶液. .
.
 .D→兔耳草醛的反應類型是加成反應.
.D→兔耳草醛的反應類型是加成反應. 、
、 .
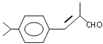
. 分析 C發生氧化反應生成兔耳草醛,根據兔耳草醛結構簡式知,C結構簡式為 ;根據題給信息知,枯茗醛和X發生加成反應生成A,A發生消去反應生成B,B發生加成反應生成C,從A到兔耳草醛其碳原子個數不變,則X為CH3CH2CHO,A為
;根據題給信息知,枯茗醛和X發生加成反應生成A,A發生消去反應生成B,B發生加成反應生成C,從A到兔耳草醛其碳原子個數不變,則X為CH3CH2CHO,A為 ,A→B發生醇的消去反應,生成B為
,A→B發生醇的消去反應,生成B為 ,B→C發生加成反應;
,B→C發生加成反應;
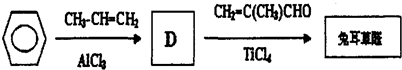
最新研究的兔耳草醛的合成路線中,苯與丙烯發生加成反應生成D,D為 ,D→兔耳草醛發生加成反應,據此分析解答.
,D→兔耳草醛發生加成反應,據此分析解答.
解答 解:C發生氧化反應生成兔耳草醛,根據兔耳草醛結構簡式知,C結構簡式為 ;根據題給信息知,枯茗醛和X發生加成反應生成A,A發生消去反應生成B,B發生加成反應生成C,從A到兔耳草醛其碳原子個數不變,則X為CH3CH2CHO,A為
;根據題給信息知,枯茗醛和X發生加成反應生成A,A發生消去反應生成B,B發生加成反應生成C,從A到兔耳草醛其碳原子個數不變,則X為CH3CH2CHO,A為 ,A→B發生醇的消去反應,生成B為
,A→B發生醇的消去反應,生成B為 ,B→C發生加成反應;
,B→C發生加成反應;
最新研究的兔耳草醛的合成路線中,苯與丙烯發生加成反應生成D,D為 ,D→兔耳草醛發生加成反應,
,D→兔耳草醛發生加成反應,
(1)通過以上分析知,X結構簡式為,故答案為:CH3CH2CHO;
(2)由上述分析可知,B為 ,含-CHO和碳碳雙鍵,均能被強氧化劑氧化,而-CHO可被弱氧化劑氧化,則先加新制氫氧化銅懸濁液檢驗-CHO,酸化后利用溴水或高錳酸鉀溶液檢驗碳碳雙鍵,
,含-CHO和碳碳雙鍵,均能被強氧化劑氧化,而-CHO可被弱氧化劑氧化,則先加新制氫氧化銅懸濁液檢驗-CHO,酸化后利用溴水或高錳酸鉀溶液檢驗碳碳雙鍵,
故答案為: ;新制氫氧化銅懸濁液;溴水或高錳酸鉀溶液;
;新制氫氧化銅懸濁液;溴水或高錳酸鉀溶液;
(3)在Cu作催化劑、加熱條件下,C發生氧化反應生成兔耳草醛,反應方程式為 ,
,
故答案為: ;
;
(4)通過以上分析知,D為 ,D發生加成反應生成兔耳草醛,故答案為:
,D發生加成反應生成兔耳草醛,故答案為: ;加成反應;
;加成反應;
(5)芳香族化合物Y與枯茗醛互為同分異構體,Y具有如下特征:
a.不能發生銀鏡反應,可發生消去反應,說明不含醛基但含有羥基;b.
核磁共振氫譜顯示:Y消去反應產物的環上只存在一種化學環境的氫原子,說明Y發生消去反應產物的環上只有一種類型氫原子,Y可能的結構簡式為 或
或 ,
,
故答案為: ;
; .
.
點評 本題考查有機物推斷,為高考高頻點,根據反應條件、部分有機物結構簡式結合題給信息進行推斷即可,側重考查學生分析推斷及知識遷移能力,明確醛之間發生加成反應時斷鍵和成鍵方式,難點是同分異構體種類判斷,題目難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
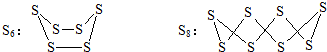
| A. | 硫單質S原子間都以σ鍵結合 | |
| B. | S6、S8分子中所有S原子都發生了sp3雜化 | |
| C. | S6和S8互為同位素 | |
| D. | 熔點的高低:S8>S6>S4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
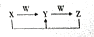 A、B、C、D、E均是常見短周期元素,其在周期表中的位置如圖.
A、B、C、D、E均是常見短周期元素,其在周期表中的位置如圖. | A | |||||
| B | C | D | |||
| E | |||||
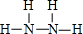
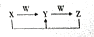 ,其中Y和Z在水溶液中存在的微粒種類相同.
,其中Y和Z在水溶液中存在的微粒種類相同.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
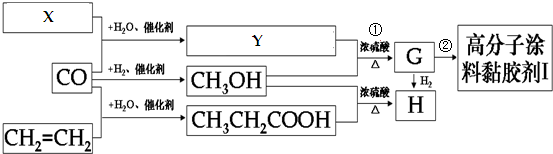
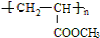
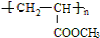 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
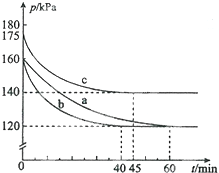 化合物AX3和單質X2在一定條件下反應可生成化合物AX5,該反應不能徹底.回答下列問題:
化合物AX3和單質X2在一定條件下反應可生成化合物AX5,該反應不能徹底.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向氯化銀的濁液中加入氯化鈉溶液,氯化銀的Ksp減小 | |
| B. | 向2.0×10-4 mol/L的K2CrO4溶液中加入等體積的2.0×10-4mol/AgNO3溶液后,則有Ag2CrO4沉淀生成 | |
| C. | 將一定量的AgCl和Ag2CrO4固體混合物溶于蒸餾水中,充分溶解后,靜置,上層清液中的Cl的物質的量濃度最大 | |
| D. | 將0.001mol/L的AgNO3溶液逐滴滴入0.001mol/L的KCl和0.001mol/L的K2CrO4的混合溶液中,則先產生AgCl沉淀. |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 取少量硫酸亞鐵銨品體溶于水,先加入氯水,再滴入幾滴硫氰化鉀溶液,溶液變血紅色,則可證明品體的成分中含有Fe2+ | |
| B. | 用到金屬鈉時,要用鑷子取,再用小刀切下所需量,剩余鈉不能放回原試劑瓶中 | |
| C. | 用pH計分別測定0.1mol•L-1的FeCl3和0.01mol•L-1FeCl3的pH,可以比較濃度對鹽類水解程度的影響 | |
| D. | 通過測定等物質的量濃度的NaCl、Na2S溶液的pH,比較硫、氯兩種元素的非金屬性強弱 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
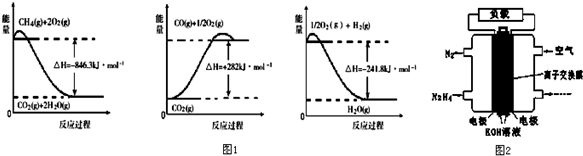
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com