

分析 Ⅰ.問題1:鐵和銅都有變價,具有相似點,正二價鐵的穩定性小于正三價的鐵,探究正一價銅的穩定性是否也小于正二價的銅,解決問題取一定量制得的氫氧化銅固體,于坩堝中灼燒,當溫度達到80~100℃得到黑色固體粉末,繼續加熱至1000℃以上,黑色粉末全部變成紅色粉末氧化亞銅,說明高溫時,+1價的銅比+2價的銅穩定,取適量紅色氧化亞銅粉末于潔凈試管中,加入過量的稀硫酸(或鹽酸),Cu2O+2H+=Cu2++Cu+H2O得到藍色溶液,同時觀察到試管底部還有紅色固體存在,說明溶液中,+2價的銅比+1價的銅穩定.
(1)根據信息:紅色氧化亞銅粉末于潔凈試管中,加入過量的稀硫酸(或鹽酸),得到藍色溶液為+2價的銅鹽溶液,同時觀察到試管底部還有紅色固體存在為銅單質,據此書寫化學方程式;
(2)根據信息:氫氧化銅固體,于坩堝中灼燒,當溫度達到80~100℃得到黑色固體粉末為氧化銅;繼續加熱至1000℃以上,黑色粉末全部變成紅色粉末氧化亞銅,說明高溫+1價銅穩定;
Ⅱ.A中堿石灰可吸收水蒸氣,C中N2H4和氧化銅反應:2CuO+N2H4$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+N2↑+2H2O,無水硫酸銅遇水變藍,可檢驗水,吸收水,B裝置增重0.36g,即生成0.02mol的水,單質氣體Y為氮氣.
(1)根據原子守恒確定氣態氫化物的化學式,計算摩爾質量;
(2)根據實驗現象來書寫化學方程式.
解答 解:Ⅰ.問題1:鐵和銅都有變價,具有相似點,正二價鐵的穩定性小于正三價的鐵,探究正一價銅的穩定性是否也小于正二價的銅,解決問題取一定量制得的氫氧化銅固體,于坩堝中灼燒,當溫度達到80~100℃得到黑色固體粉末,繼續加熱至1000℃以上,黑色粉末全部變成紅色粉末氧化亞銅,說明高溫時,+1價的銅比+2價的銅穩定,取適量紅色氧化亞銅粉末于潔凈試管中,加入過量的稀硫酸(或鹽酸),Cu2O+2H+=Cu2++Cu+H2O得到藍色溶液,同時觀察到試管底部還有紅色固體存在,說明溶液中,+2價的銅比+1價的銅穩定.
(1)根據信息:紅色氧化亞銅粉末于潔凈試管中,加入過量的稀硫酸(或鹽酸),得到藍色溶液為+2價的銅鹽溶液,同時觀察到試管底部還有紅色固體為銅單質,Cu2O中+1價的銅在酸性溶液中發生氧化還原反應:Cu2O+2H+=Cu+Cu2++H2O,
故答案為:Cu2O+2H+=Cu+Cu2++H2O;
(2)根據信息:氫氧化銅固體,于坩堝中灼燒,當溫度達到80~100℃得到黑色固體粉末;繼續加熱至1000℃以上,黑色粉末全部變成紅色粉末氧化亞銅,根據在不同溫度下反應物的組成可確定物質的穩定性,所以高于1000℃時Cu2O比CuO穩定,在溶液中:Cu2O+2H+=Cu+Cu2++H2O,所以Cu2+比Cu+穩定,
故答案為:高溫時,+1價的銅比+2價的銅穩定,而溶液中,+2價的銅比+1價的銅穩定;
Ⅱ.(1)消耗0.01mol X,測得B裝置增重0.36g,即生成0.02mol的水,并收集到單質氣體Y 0.28g即氮氣0.01mol,根據原子守恒可以確定氣態氫化物X中含有4個氫原子和2個氮原子,X的化學式為N2H4,其摩爾質量為32g/mol,
故答案為:32g/mol;
(2)C中發生反應的化學方程式為N2H4和氧化銅反應:2CuO+N2H4$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+N2↑+2H2O,
故答案為:2CuO+N2H4$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+N2↑+2H2O.
點評 本題考查實驗探究和數據處理,做題時注意變價金屬氧化物的性質以及質量守恒定律計算物質的化學式.題目難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
| 時間(s) c(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(A) | 0.20 | 0.14 | b | 0.09 | 0.09 | 0.09 |
| c(B) | 0.00 | 0.12 | 0.20 | c | d | e |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 乙酸異戊脂是組成蜜蜂信息素質的成分之一,具有香蕉的香味,實驗室制備乙酸異戊酯的反應裝置示意圖圖1和有關數據如下:
乙酸異戊脂是組成蜜蜂信息素質的成分之一,具有香蕉的香味,實驗室制備乙酸異戊酯的反應裝置示意圖圖1和有關數據如下: +
+ $?_{△}^{濃H_{2}SO_{4}}$
$?_{△}^{濃H_{2}SO_{4}}$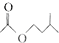 +H2O
+H2O| 相對分子質量 | 密度/(g.cm-3) | 沸點/℃ | 水中溶解性 | |
| 異戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙醇 | 60 | 1.0492 | 118 | 溶 |
| 乙醇異戊酯 | 130 | 0.8670 | 142 | 難溶 |

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 二甲醚(CH3OCH3)被稱為21世紀的新型燃料,在未來可能替代汽油、液化氣、煤氣等并具有優良的環保性能.工業制備二甲醚在催化反應室中(壓力2.0~10.0Mpa,溫度230~280℃)進行下列反應:
二甲醚(CH3OCH3)被稱為21世紀的新型燃料,在未來可能替代汽油、液化氣、煤氣等并具有優良的環保性能.工業制備二甲醚在催化反應室中(壓力2.0~10.0Mpa,溫度230~280℃)進行下列反應:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | K+、Na+、SO42-、Mn2+ | B. | Cl-、S2-、Fe2+、H+ | ||
| C. | Na+、Ba2+、Br-、CO32- | D. | Na+、H+、NO3-、HCO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 如圖中相連的兩種物質均可歸為一類,相交的部分A、B、C、D為其相應的分類標準代號,請回答下列問題:
如圖中相連的兩種物質均可歸為一類,相交的部分A、B、C、D為其相應的分類標準代號,請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 焓減小的反應通常是自發的,能夠自發進行的反應都是焓減小的反應 | |
| B. | 熵增加的反應通常是自發的,能夠自發進行的反應都是熵增加的反應 | |
| C. | 常溫下,反應C(s)+CO2(g)═2CO(g)不能自發進行,則該反應的△H>0 | |
| D. | △G<0的反應是自發的,因此在任何條件均可發生 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SO2的摩爾質量是64g | |
| B. | 1molSO2中所含分子數約為6.02×1023 | |
| C. | 1molSO2的質量是64g/mol | |
| D. | 常溫常壓下,1mol SO2的體積為22.4L |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com