
| 熔點/K | 沸點/K | 標準狀況時在水中的溶解度 | |
| 甲 | 187 | 202 | 2.6 |
| 乙 | 272.26 | 425.25 | 以任意比互溶 |
分析 (1)Cu是29號元素,原子核外電子數為29,根據核外電子排布規(guī)律書寫核外電子排布式;
(2)硫酸銅先和氨水反應生成氫氧化銅,氫氧化銅和氨水反應生成絡合物,根據反應寫出離子反應方程式;硫酸四氨合銅在乙醇中的溶解度遠小于在水中的溶解度向溶液中加入乙醇后析出藍色晶體硫酸四氨合銅;
(3)根據題目信息可知甲為H2S,乙為H2O2,丙為C2H6,
①1個H2O2中含有3個共價單鍵,即3個個σ鍵;
②對于有機物利用雜化軌道數=孤對電子對數+σ鍵數進行判斷;
③H2O2分子間存在氫鍵以及H2O2分子與水分子可形成氫鍵來解答.
解答 解:(1)Cu是29號元素,原子核外電子數為29,基態(tài)原子核外電子排布式為:1s22s22p63s23p63d104s1,
故答案為:1s22s22p63s23p63d104s1;
(2)氨水和硫酸銅反應生成氫氧化銅藍色沉淀,當氨水過量時,氨水和氫氧化銅反應生成可溶性的銅氨絡合物,所以難溶物溶解得到深藍色的透明溶液,涉及的離子方程式為:Cu2++2NH3•H2O═Cu(OH)2↓+2NH4+、Cu(OH)2+4NH3═[Cu(NH3)4]2++2OH-,總反應為:Cu2++4NH3•H2O═[Cu(NH3)4]2++4H2O、或Cu2++4NH3=[Cu(NH3)4]2+;硫酸四氨合銅在乙醇中的溶解度遠小于在水中的溶解度向溶液中加入乙醇后析出藍色晶體硫酸四氨合銅,
故答案為:Cu2++4NH3•H2O=[Cu(NH3)4]2++4H2O或Cu2++4NH3=[Cu(NH3)4]2+;析出藍色晶體;硫酸四氨合銅在乙醇中的溶解度遠小于在水中的溶解度;
(3)①1個H2O2中含有3個共價單鍵,即3個個σ鍵,所以1molH2O2分子含有3NA個σ鍵,故答案為:3NA;
②C2H6分子中碳原子形成3個C-H,1個C-C雙鍵,C原子雜化軌道數為(3+1)=4,C原子采取sp3雜化方式,故答案為:sp3;
③H2O2分子間存在氫鍵,所以熔沸點比H2S高;H2O2分子與水分子可形成氫鍵,所以與任意比互溶,故答案為:H2O2分子間存在氫鍵,因此熔沸點更高;H2O2與水分子可形成氫鍵,可以與水任意比互溶.
點評 本題考查物質結構與性質,明確原子序數、電子排布、配合物的性質、雜化理論等知識是解答關鍵,題目難度中等.


 奪冠訓練單元期末沖刺100分系列答案
奪冠訓練單元期末沖刺100分系列答案 新思維小冠軍100分作業(yè)本系列答案
新思維小冠軍100分作業(yè)本系列答案 名師指導一卷通系列答案
名師指導一卷通系列答案科目:高中化學 來源: 題型:解答題
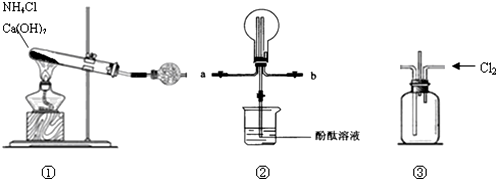
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
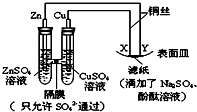
| A. | Y為陰極,發(fā)生還原反應 | B. | X為正極,發(fā)生氧化反應 | ||
| C. | 鋅電極表面有紅色的銅析出 | D. | X與濾紙接觸處變紅 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,1mol固體氫氧化鈉的體積比1mol氫氣的體積小 | |
| B. | NA個氧氣分子和NA個氫氣分子的質量比為16:l | |
| C. | 28g氮氣所含的原子數目為NA | |
| D. | NA個H2SO4分子中所含氧原子個數與4NA個H2O分子中所含氧原子個數相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 稀H2SO4 | B. | CuSO4溶液 | C. | AgNO3溶液 | D. | Fe2(SO4)3溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,16g O2和32g O3的混合物中,含有O原子數目為3NA | |
| B. | 標準狀態(tài)下,1mol Na2O和1mol Na2O2的混合物中,含有離子總數為7NA | |
| C. | 1mol NaHSO4溶于水或受熱熔化,電離出來的離子數目均為2NA | |
| D. | 在K35ClO3+6H37Cl=KCl+3Cl2↑+3H2O中,若生成71g Cl2,轉移的電子數目為$\frac{5}{3}$NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 品名 | 蘇打餅干 |
| 配料 | 面料、鮮雞蛋、精煉食用植物油、白砂糖、奶油、食鹽、蘇打 |
| 保質期 | 12個月 |
| 生產日期 | 2015年5月15日 |
| A. | 精煉食用植物油能使溴水和酸性KMnO4溶液褪色 | |
| B. | 白砂糖屬于二糖,在人體內水解而轉化為單糖 | |
| C. | 鮮雞蛋清遇濃硝酸變?yōu)辄S色 | |
| D. | 奶油與白砂糖都是高分子化合物 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com