
 如圖轉化關系圖(反應條件均略去)中A、C、E、G均為單質,其中A、C、G為金屬;E為氣體;B為無色液體;A、G在冷的濃硫酸溶液中均發生鈍化;F、I溶液的焰色均為黃色.
如圖轉化關系圖(反應條件均略去)中A、C、E、G均為單質,其中A、C、G為金屬;E為氣體;B為無色液體;A、G在冷的濃硫酸溶液中均發生鈍化;F、I溶液的焰色均為黃色.分析 A、G在冷的濃硫酸溶液中均發生鈍化,則A、G為Al、Fe,G與D反應生成H和A,則A為Al,G為Fe,D為鐵的氧化物,H為Al2O3,B為無色液體,B為H2O,所以D為Fe3O4,E為4H2,F、I溶液的焰色均為黃色,則F、I中含有鈉元素,C為金屬,所以C為Na,F為NaOH,鋁與氫氧化鈉的水溶液反應生成I和E,所以I為NaAlO2,據此答題.
解答 解:A、G在冷的濃硫酸溶液中均發生鈍化,則A、G為Al、Fe,G與D反應生成H和A,則A為Al,G為Fe,D為鐵的氧化物,H為Al2O3,B為無色液體,B為H2O,所以D為Fe3O4,E為4H2,F、I溶液的焰色均為黃色,則F、I中含有鈉元素,C為金屬,所以C為Na,F為NaOH,鋁與氫氧化鈉的水溶液反應生成I和E,所以I為NaAlO2,
(1)反應①為鐵與水蒸汽反應生成四氧化三鐵和氫氣,反應的化學方程式為3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$ Fe3O4+4H2,
故答案為:3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$ Fe3O4+4H2;
(2)反應④的離子方程式為 2Al+2H2O+2OH-=2AlO2-+3H2↑,
故答案為:2Al+2H2O+2OH-=2AlO2-+3H2↑;
(3)反應③后所得 Fe中含有少量物質Al和Al2O3,其中Al和Al2O3能和氫氧化鈉反應,而鐵不反應,所以除去A中這兩種雜質的方法是 加入足量NaOH溶液反應后過濾,
故答案為:加入足量NaOH溶液反應后過濾;
(4)日常生活中鋁的制品比鐵的制品耐腐蝕的原因是在常溫下Al表面會生成致密的氧化膜,防止內部的Al進一步被氧化,而鐵不能,
故答案為:Al表面會生成致密的氧化膜,防止內部的Al進一步被氧化.
點評 本題考查無機物的推斷,轉化中特殊反應、物質的顏色、狀態等是推斷突破口,需要學生熟練掌握元素化合物知識,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | Mg2+、NH${\;}_{4}^{+}$、OH-、SO${\;}_{4}^{2-}$ | B. | Na+、H+、Cl-、HCO${\;}_{3}^{-}$ | ||
| C. | Na+、K+、AlO${\;}_{2}^{-}$、CO${\;}_{3}^{2-}$ | D. | H++、K+、MnO${\;}_{4}^{-}$、SO${\;}_{3}^{2-}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 實驗步驟 | 預期現象和結論 |
| 步驟1:取少量樣品溶于足量的鹽酸后,將溶 液分成兩份,分別裝入A、B試管中. | |
| 步驟2:用潔凈的鉑絲蘸取A中的溶液,在酒精燈火焰上灼燒,觀察焰色 | 焰色呈黃色證明有Na+,發酵粉中有NaHCO3 |
| 步驟3:向B試管中逐滴滴加0.1mol/L NaOH溶液 | 看到有白色沉淀生成(或先產生白色沉淀后沉淀溶解),證明發酵粉中有明礬. |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 打開啤酒瓶蓋后有大量泡沫溢出 | |
| B. | 實驗室用排飽和食鹽水的方法收集氯氣 | |
| C. | 熱的純堿去油污能力更強 | |
| D. | 夏天將食品儲藏在冰箱中 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


 .
. .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | B、C、D形成的簡單離子半徑大小順序Cm+>Dn+>Bx-(m+、n+、x-表示所帶電荷) | |
| B. | A、B、E氣態氫化物穩定性為E>A>B | |
| C. | C和D的最高價氧化物對應的水化物之間可以發生反應 | |
| D. | E單質是制備太陽能電池的重要材料是因為E的單質導電性強 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
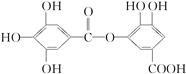 ,關于它的性質敘述中不正確的是( )
,關于它的性質敘述中不正確的是( )| A. | 酸性條件下可發生水解反應,且產物只有一種 | |
| B. | 1mol該有機物最多可跟8molNaOH反應 | |
| C. | 1mol該有機物最多可跟2molBr2反應 | |
| D. | 該有機物可跟NaHCO3溶液反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4 | B. | 3 | C. | 2 | D. | 1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com