
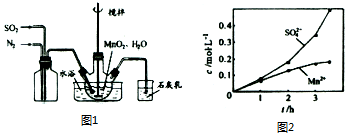
分析 (1)①根據題中所示的石灰乳的作用是吸收尾氣二氧化硫,堿和酸性氧化物反應得到對應的鹽和水,據此回答;
②根據實驗的操作原則,為了讓氣體盡可能轉化,要根據反應所需的條件和用量嚴格操作;
③考慮氮氣的化學性質穩定,空氣中氧氣的活潑性等因素的影響;
(2)制取的原理是碳酸根和錳離子之間反應生成碳酸錳的過程,但要考慮MnCO3難溶于水、乙醇并在潮濕時易被空氣氧化,100℃開始分解以及Mn(OH)2開始沉淀時pH=7.7等因素,過程中控制溶液的PH值以及洗滌沉淀所選的溶劑要小心,據此答題.
解答 解:(1)①石灰乳的作用是吸收尾氣二氧化硫,堿和酸性氧化物反應得到對應的鹽和水,反應方程式為:SO2+Ca(OH)2=CaSO3+H2O,
故答案為:SO2+Ca(OH)2=CaSO3+H2O;
②為使SO2盡可能轉化完全,應定要保證控制反應的溫度,在通入SO2和N2比例一定、不改變固液投料的條件下,要求所通氣體一定要慢,故答案為:控制適當的溫度;緩慢通入混合氣體;
③氮氣的化學性質穩定,空氣中氧氣性質活潑,在Mn2+催化作用下,易把亞硫酸氧化成硫酸,而使硫酸根濃度增大,故答案為:Mn2+催化氧氣與亞硫酸反應生成硫酸;
(2)①因為Mn(OH)2開始沉淀時pH=7.7,所以A步驟中控制溶液PH<7.7的原因可能是防止生成Mn(OH)2沉淀,離子方程式為:Mn2++2OH-=Mn(OH)2↓,故答案為:Mn2++2OH-=Mn(OH)2↓;
②檢驗SO42-是否被洗滌干凈,可以取最后一次洗滌的濾液少量于試管,加入用鹽酸酸化的BaCl2溶液,若無明顯現象,說明水洗合格,故答案為:取最后一次洗滌的濾液少量于試管,加入用鹽酸酸化的BaCl2溶液,若無明顯現象,說明水洗合格;
③用少量的乙醇洗滌,主要原因是乙醇容易揮發,便于低溫干燥,防止MnCO3 受潮被氧化,受熱分解,故答案為:乙醇容易揮發,便于低溫干燥,防止MnCO3 受潮被氧化,受熱分解.
點評 本題主要考查了制備高純碳酸錳實驗方案,讀懂工藝流程,正確識圖、理解離子反應的本質是解答的關鍵,本題實驗綜合性強,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4L氯氣與足量氫氧化鈉溶艘反應轉移的電子數為2NA | |
| B. | 將含有1molFeCl3的飽和溶液加入到沸水中得到氫氧化鐵膠體,其中膠體粒子的數目為NA | |
| C. | 兩份2.7g鋁分別與100 mL濃度為2mol•L-1的鹽酸和氫氧化鈉溶液充分反應,轉移的電子數均為0.3NA | |
| D. | 通常情況下,16g CH4中含有4NA個C-H鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A | B | C | D | |
| 化合物 | HCl | NaOH | Cu2(OH)2SO4 | FeSO4•7H2O |
| 氧化物 | H2O | Na2O | CO | Fe3O4 |
| 電解質 | 食鹽水 | SO2 | H2SO4 | 鐵 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C3N4 晶體是分子晶體 | |
| B. | C3N4 晶體中微粒間通過離子鍵結合 | |
| C. | C3N4 晶體中C-N鍵的鍵長比金剛石中C-C鍵的鍵長要長 | |
| D. | C3N4 晶體中每個C原子連接4個N 原子,而每個N原子連接3個C原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
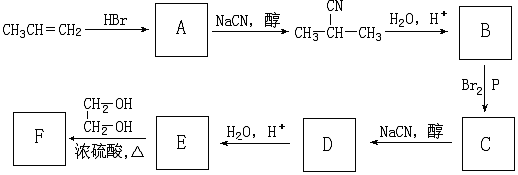
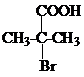 +NaCN$\stackrel{醇}{→}$NaBr+
+NaCN$\stackrel{醇}{→}$NaBr+ ,E→F(F為高分子時)nHOOC-C(CH3)2-COOH+nHOCH2CH2OH$→_{△}^{濃硫酸}$
,E→F(F為高分子時)nHOOC-C(CH3)2-COOH+nHOCH2CH2OH$→_{△}^{濃硫酸}$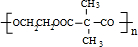 +2nH2O.
+2nH2O.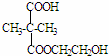 ,②分子內含有一個七元環
,②分子內含有一個七元環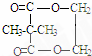 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 水晶、瑪瑙、紅寶石、藍寶石的主要成分都是非金屬氧化物 | |
| B. | 蛋白質是結構復雜的高分子化合物,蛋白質的生物活性首先取決于蛋白質的一級結構 | |
| C. | 同位素示蹤法是研究化學反應歷程的手段之一,紅外光譜法可用于研究有機物分子結構,滴定法不能用于測量鹽類物質溶液的濃度 | |
| D. | 丁達爾現象可用于區別溶液與膠體,云、霧、稀硫酸均能產生丁達爾現象 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 操作和現象 | 結論或目的 | |
| A | 向純堿中滴加足量濃鹽酸,將所得氣體通入硅酸鈉溶液中,溶液變渾濁 | 酸性:鹽酸>碳酸>苯酚 |
| B | 取某溶液少量,加入鹽酸酸化的氯化鋇溶液,出現白色沉淀 | 該溶液中一定含有大量的SO42- |
| C | 取少量Fe(NO3)2試樣加水溶液后加稀硫酸酸化,滴加KSCN溶液,溶液變為紅色 | 該Fe(NO3)2試樣已經變質 |
| D | 處理鍋爐水垢中的CaSO4時,依次加入飽和Na2CO3溶液和鹽酸,水垢溶解 | 目的:將不溶于酸的沉淀轉化為易溶于酸的沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 12g由${\;}_{6}^{12}$C60和${\;}_{6}^{14}$C60組成的固體中的原子數為NA | |
| B. | 4.4g由CO2和N2O組成的混合氣體中的電子數為2.2NA | |
| C. | 常溫常壓下22.4LNH3中所含的共價鍵數為3NA | |
| D. | 1L1mol•L-1次氯酸溶液中的ClO-數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 化學鍵 | N≡O | Cl-Cl | Cl-N | N=O |
| 鍵能/kJ.mol-1 | 630 | 243 | a | 607 |
| 序號 | c(ClNO)/mol.L-1 | v/mol.L-1•s-1 |
| ① | 0.30 | 3.60×10${\;}^{-{9}^{\;}}$ |
| ② | 0.60 | 1.44×10-8 |
| ③ | 0.90 | 3.24×10-8 |
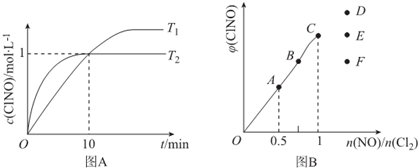
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com