
| A. | 稀硫酸滴在銅片上:Cu+2H+═Cu2++H2 | |
| B. | 氧化銅與硫酸反應:O2-+2 H+═H2O | |
| C. | 硫酸鈉和氯化鋇兩種溶液混合:Ba2++SO42-═BaSO4↓ | |
| D. | 鹽酸與石灰石反應:CaCO3+2H+═Ca2++H2O+CO2↑ |
分析 A.Cu與稀硫酸不反應;
B.CuO在離子反應中保留化學式;
C.反應生成硫酸鋇和氯化鈉;
D.反應生成氯化鈣、水、二氧化碳.
解答 解:A.稀硫酸滴在銅片上,不發生反應,故A錯誤;
B.氧化銅與硫酸反應的離子反應為CuO+2H+═Cu2++H2O,故B錯誤;
C.硫酸鈉和氯化鋇兩種溶液混合的離子反應為Ba2++SO42-═BaSO4↓,故C正確;
D.鹽酸與石灰石反應的離子反應為CaCO3+2H+═Ca2++H2O+CO2↑,故D正確;
故選CD.
點評 本題考查離子反應方程式書寫的正誤判斷,為高頻考點,把握發生的反應及離子反應的書寫方法為解答的關鍵,側重分析與應用能力的考查,注意離子反應中保留化學式的物質,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | Y元素最高價氧化物對應的水化物化學式為H3YO4 | |
| B. | 原子半徑由大到小的順序為W>Z>Y>X | |
| C. | X、Z兩種元素的氧化物中所含化學鍵類型相同 | |
| D. | 與同濃度的鹽酸反應,Z比W更劇烈 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
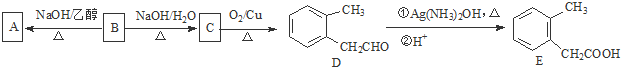
 .
.
 (或
(或 、
、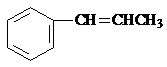 ) .
) .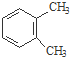 $→_{一定條件}^{Cl_{2}}$
$→_{一定條件}^{Cl_{2}}$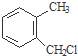 $→_{③}^{NaCN}$
$→_{③}^{NaCN}$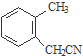 $→_{H_{2}O}^{H_{2}SO_{4}}$
$→_{H_{2}O}^{H_{2}SO_{4}}$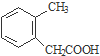
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 陶瓷不屬于金屬材料 | |
| B. | 鈉鉀合金的熔點介于鈉和鉀的熔點之間 | |
| C. | 純鐵比生鐵的硬度大 | |
| D. | 鋁在常溫下不能與氧氣反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
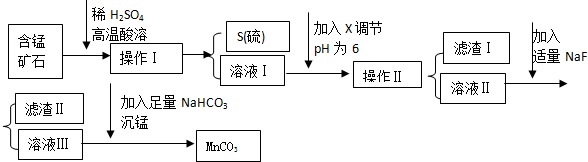
| 物質 | 開始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Ca(OH)2 | 12 | ------ |
| Al(OH)3 | 3.8 | 4.7 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 硫酸的摩爾質量是98 g•mol-1 | |
| B. | 2 mol NO和1 mo1 NO2所含的氧元素質量相同 | |
| C. | 等質量的02和03所含氧原子數相等 | |
| D. | 等物質的量的CO和CO2所含氧原子數相等 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com