
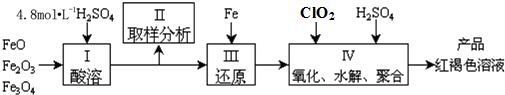
分析 (1)實驗室用18.4mol•L-1的濃硫酸配制250mL4.8mol•L-1的硫酸溶液,所需的玻璃儀器有量筒、燒杯、玻璃棒、250mL容量瓶、膠頭滴管;
(2)控制水解時Fe3+的濃度,防止生成氫氧化鐵沉淀,原料中的Fe3+必須先還原為Fe2+,所以確定下一步還原所需鐵的量,然后Fe2+再被ClO2氧化為Fe3+;
(3)酸性條件下,ClO2將Fe2+氧化為Fe3+,ClO2被還原為Cl-;
(4)①氧化劑氧化性強于氧化產物氧化性;
②mg白色沉淀為BaSO4,由硫酸根守恒n(SO42-)=n(BaSO4),由原子守恒與電電子轉移守恒可得關系式:5Fe3+~5Fe2+~MnO4-,根據關系式計算n(Fe3+).
解答 解:(1)實驗室用18.4mol•L-1的濃硫酸配制250mL4.8mol•L-1的硫酸溶液,用量筒量取濃硫酸,在燒杯中溶解,并用玻璃棒攪拌,移入2500mL容量瓶,最后需要用膠頭滴管定容,
故答案為:250mL容量瓶、膠頭滴管;
(2)因為控制水解時Fe3+的濃度,防止生成氫氧化鐵沉淀,原料中的Fe3+必須先還原為Fe2+,所以確定下一步還原所需鐵的量,然后Fe2+再被氧化Fe3+,需要確定氧化Fe2+所需ClO2的量,
故答案為:AC;
(3)酸性條件下,ClO2將Fe2+氧化為Fe3+,ClO2被還原為Cl-,反應離子方程式為:5Fe2++ClO2+4H+=5Fe3++Cl-+2H2O,
故答案為:5Fe2++ClO2+4H+=5Fe3++Cl-+2H2O;
(4)①發生反應:Cu+2Fe3+=2Fe2++Cu2+,5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,氧化劑氧化性強于氧化產物氧化性,氧化性由強到弱的順序:MnO4->Fe3+>Cu2+>Fe2+,
故答案為:MnO4->Fe3+>Cu2+>Fe2+;
②mg白色沉淀為BaSO4,由硫酸根守恒n(SO42-)=n(BaSO4)=$\frac{m}{233}$mol,由原子守恒與電電子轉移守恒可得關系式:5Fe3+~5Fe2+~MnO4-,則n(Fe3+)=5n(MnO4-)=5×V×10-3L×0.1mol/L×$\frac{250mL}{25mL}$,
n(SO42-):n(Fe3+)=$\frac{m}{233}$mol:5×V×10-3L×0.1mol/L×$\frac{250mL}{25mL}$=$\frac{m}{233}$:$\frac{V}{200}$,
故答案為:$\frac{m}{233}$:$\frac{V}{200}$.
點評 本題以聚合硫酸鐵的制備為載體,考查溶液配制、氧化還原反應配平、氧化性強弱比較、化學工藝流程等,是對學生綜合能力的考查,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 工業上用電解熔融氯化鎂制單質鎂 | |
| B. | 工業上用電解飽和食鹽水制氯氣 | |
| C. | 工業上用二氧化硅在高溫下與焦炭反應制得高純度的硅 | |
| D. | 工業上煉鐵時,常用石灰石除去鐵礦石中的SiO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 烷烴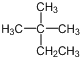 的系統命名為2-甲基-2-乙基丙烷 的系統命名為2-甲基-2-乙基丙烷 | |
| B. | 甲苯苯環上的一個氫原子被含4個碳原子的烷基取代,所得產物有12種 | |
| C. | 乙烯能使溴的四氯化碳溶液和酸性高錳酸鉀溶液褪色,其原理相同 | |
| D. | 在堿性條件下,CH3CO18OC2H5的水解產物是CH3COOH和C2H518OH |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.5mol•L-1CuCl2溶液含有3.01×1023個Cu2+ | |
| B. | 28g聚乙烯分子含有的碳原子數為 NA | |
| C. | 0.2mol PCl5分子中,鍵數目為NA | |
| D. | 標準狀況下,3.36L H2O含有9.03×1023個H2O分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 步驟編號 | 操作過程 | 實驗現象 | 實驗結論 |
| ① | 氯水有酸性 | ||
| ② | 氯水有漂白性 | ||
| ③ | 氯水中存在Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com