
| A. | 工業上用電解熔融氯化鎂制單質鎂 | |
| B. | 工業上用電解飽和食鹽水制氯氣 | |
| C. | 工業上用二氧化硅在高溫下與焦炭反應制得高純度的硅 | |
| D. | 工業上煉鐵時,常用石灰石除去鐵礦石中的SiO2 |
分析 A.工業上用電解熔融氯化鎂的方法制取鎂;
B.用電解飽和食鹽水制氯氣,氫離子和氯離子放電;
C.生成一氧化碳和粗硅;
D.高爐煉鐵時,使用石灰石的目的是:將礦石中的二氧化硅轉變為爐渣,即除去脈石(SiO2).
解答 解:A.工業上用電解熔融氯化鎂的方法制取鎂,可用于工業生產,故A正確;
B.用電解飽和食鹽水制氯氣,氫離子和氯離子放電,可用于工業生產,故B正確;
C.二氧化硅和與碳在高溫下發生置換反應,生成一氧化碳和粗硅,得不到高純度硅,故C錯誤;
D.煉鐵時,石灰石中的碳酸鈣在高溫條件下分解能生成氧化鈣和二氧化碳,氧化鈣能和二氧化硅反應生成硅酸鈣,從而除去鐵礦石中的二氧化硅,可用于工業生產,故D正確.
故選C.
點評 本題考查了有關化學工藝的一些知識,掌握從海水中提取金屬鎂原理、氯氣制備原理、制取高純硅的原理以及工業煉鐵除去鐵礦石中的脈石方法原理是解答的關鍵,題目難度中等.


 中考解讀考點精練系列答案
中考解讀考點精練系列答案科目:高中化學 來源: 題型:解答題

| 金屬離子 | Fe3+ | Cu2+ |
| 氫氧化物開始沉淀時的pH | 1.9 | 4.7 |
| 氫氧化物完全沉淀時的pH | 3.2 | 6.7 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 可能由pH=2的鹽酸與pH=12的氨水等體積混合而成 | |
| B. | 該溶液可能由等物質的量濃度的鹽酸和氨水等體積混合而成 | |
| C. | 加入適量氨水,溶液中離子濃度可能為:c (NH4+)>c (Cl-)>c (OH-)>c(H+) | |
| D. | 該溶液中c (NH4+)=c (Cl-)+c (OH-)-c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
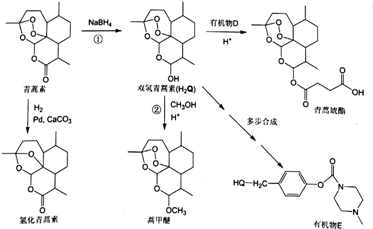
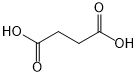 (或
(或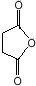 ).
). .
.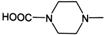 外,還需含苯環的二羥基化合物P,其結構簡式為
外,還需含苯環的二羥基化合物P,其結構簡式為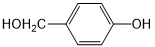 .化合物S是P的同分異構體,其分子結構含有苯環,有4種不同類型的氫,且個數比為3:2:2:1,寫出S的一種結構簡式
.化合物S是P的同分異構體,其分子結構含有苯環,有4種不同類型的氫,且個數比為3:2:2:1,寫出S的一種結構簡式 (或
(或 ,其他合理答案亦可).
,其他合理答案亦可).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 裝置甲中銅片表面產生氣泡 | |
| B. | 裝置甲溶液中SO42ˉ向銅片做定向移動 | |
| C. | 裝置乙中電子從銅片經導線流向鋅片 | |
| D. | 裝置乙中正極的電極反應式:2H++2eˉ═H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 配制一定物質的量濃度的溶液,向容量瓶加水至液面離刻度線1~2 cm時,改用膠頭滴管定容 | |
| B. | 向某溶液中先加入Ba(NO3)2溶液,再加入足量的HNO3溶液,產生白色沉淀,則該溶液中一定含有SO42- | |
| C. | 分液操作時,將下層液體先放出,然后關閉旋塞,將上層液體從上口倒出 | |
| D. | 將油脂與氫氧化鈉溶液混合充分反應后,再加入熱的飽和食鹽水,則可析出肥皂的主要成分 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
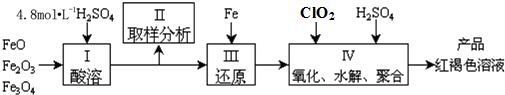
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲烷的燃燒熱為890.3kJ•mol-1,則甲烷燃燒的熱化學方程式可表示為:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| B. | 500℃、30MPa下,將0.5mol N2和1.5molH2置于密閉的容器中充分反應生成NH3(g),放熱19.3kJ,其熱化學方程式為:N2(g)+3H2(g)$?_{500℃、30MPa}^{催化劑}$2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 向Na2CO3溶液中滴入酚酞溶液,溶液變紅:CO32-+2H2O?H2CO3+2OH- | |
| D. | 純水的電離方程式:H2O+H2O?H3O++OH- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com