
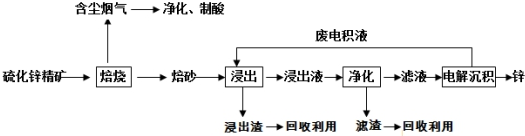
分析 硫化鋅精礦的焙燒可生成ZnO、氧化鐵等,含塵煙氣含有含硫氧化物,可用于制備硫酸,浸出液加入硫酸可生成硫酸鋅、硫酸鐵,加入過量鋅充分反應,可置換出鐵,濾液中主要含有硫酸鋅,經電解可得到鋅和硫酸,電解液中含有硫酸,可循環利用.
(1)含鋅礦的主要成分是ZnS,與空氣中氧氣發生氧化還原反應,判斷焙砂的主要成分為氧化鋅;
(2)焙燒生成的含硫氧化物可轉換為硫酸;
(3)該含鋅礦中還含有FeS等雜質,浸出操作后轉化為亞鐵離子,可加入鋅粉出去亞鐵離子,從而除去Fe;
(4)電解沉積過程中,是電解ZnSO4,陽極上是氫氧根離子失電子發生氧化反應;
(5)“氧壓酸浸”法顧名思義,可知反應物中含有H+和O2,可以獲得非金屬單質S,根據反應物和生成物寫出化學方程式;
(6)根據沉淀的轉化原理可知,在一定條件下,溶解度小的礦物可以轉化為溶解度更小的礦物;
(7)根據題目描述可知反應物為ZnCO3和C,產物含有Zn,根據反應物和生成物寫出化學方程式.
解答 解:(1)含鋅礦的主要成分是ZnS,與空氣中氧氣發生氧化還原反應,則焙砂的主要成分為ZnO,
故答案為:ZnO;
(2)焙燒生成的含硫氧化物可轉換為硫酸,用于后續的浸出操作,
故答案為:浸出;
(3)該含鋅礦中還含有FeS等雜質,浸出操作后轉化為亞鐵離子,可加入鋅粉出去亞鐵離子,從而除去Fe,反應的離子方程式為Zn+Fe2+=Zn2++Fe,
故答案為:置換出Fe等;Zn+Fe2+=Zn2++Fe;
(4)電解沉積過程中,是電解ZnSO4,陰極鋅離子放電生成鋅,陽極發生氧化反應,產物為O2,故答案為:O2;
(5)“氧壓酸浸”法顧名思義,可知反應物中含有H+和O2,可以獲得非金屬單質S,寫出化學方程式為:2ZnS+4H++O2=2Zn2++2S↓+2H2O;
故答案為:2ZnS+4H++O2=2Zn2++2S↓+2H2O;
(6)根據沉淀的轉化原理可知,在一定條件下,溶解度小的礦物可以轉化為溶解度更小的礦物,所以硫化鋅精礦(ZnS)遇到硫酸銅溶液可慢慢地轉變為銅藍(CuS),
故答案為:在一定條件下,溶解度小的礦物可以轉化為溶解度更小的礦物(或在相同條件下,由于KSP(CuS)小于KSP(ZnS),故反應可以發生);
(7)根據題目描述可知反應物為ZnCO3和C,產物含有Zn,則化學方程式為ZnCO3+2C$\frac{\underline{\;高溫\;}}{\;}$Zn+3CO↑,故答案為:ZnCO3+2C$\frac{\underline{\;高溫\;}}{\;}$Zn+3CO↑.
點評 本題為工藝流程題,為高頻考點,側重于學生的分析能力和實驗能力的考查,題目通過鋅的煉制考查了化學方程式、離子方程式的書寫,明確工藝流程及各種物質的性質是解題關鍵,題目難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題

| A. | 向a試管中先加入濃硫酸,然后邊搖動試管邊慢慢加入乙醇,再加冰醋酸 | |
| B. | 試管b中導氣管下端管口不能浸入液面的原因是防止實驗過程中發生倒吸現象 | |
| C. | 實驗時加熱試管a的目的是及時將乙酸乙酯蒸出并加快反應速率 | |
| D. | 試管b中Na2CO3的作用是除去隨乙酸乙酯蒸出的少量乙酸和乙醇,降低乙酸乙酯在溶液中的溶解度 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ${\;}_{48}^{112}$Cd原子的中子數為64 | |
| B. | 聚氯化鋁能降污是因為它有強氧化性 | |
| C. | 聚氯化鋁是混合物 | |
| D. | 鎘的單質有導電性和延展性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 體積大小:③>②>① | B. | 原子數目:③>①>② | C. | 密度大小:②>③>① | D. | 質量大小:②>①>③ |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com