
一定條件下反應2AB(g) 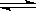 A2(g)+B2(g)達到平衡狀態的標志是( )
A2(g)+B2(g)達到平衡狀態的標志是( )
A.單位時間內生成 nmolA2的同時消耗n molAB
nmolA2的同時消耗n molAB
B.容器內,3種氣體AB、A2、B2共存
C.AB的消耗速率等于A2的消耗速率
D.容器中各組分的體積分數不隨時間變化
科目:高中化學 來源: 題型:解答題
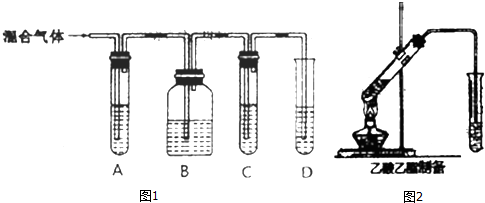
 CH3COOCH2CH3+H2O,該反應類型為酯化反應(取代反應).
CH3COOCH2CH3+H2O,該反應類型為酯化反應(取代反應).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 現象相同,沉淀量相等 | B. | 現象相同,沉淀量不等 | ||
| C. | 現象不同,沉淀量相等 | D. | 現象不同,沉淀量不等 |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上10月月考化學試卷(解析版) 題型:選擇題
把溫度為20℃,濃度為1.0mol·L-1的H2SO4和2.2mol·L-1的堿溶液各50ml混合(溶液密度均為1g·ml-1,比熱容為4.184kJ·K-1·kg-1),輕輕攪動。測得酸堿混合液的溫度變化數據如下:
反應物 | 起始溫度t1℃ | 終止溫度t2℃ |
H2SO4+NaOH | 20 | 33.6 |
H2SO4+NH3·H2O | 20 | 32.6 |
則反應NH3·H2O=NH4++OH-的焓變約為( )(單位:kJ·mol-1)
A.2.1 B.4.2 C.52.7 D. 缺少數據無法計算
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上10月月考化學試卷(解析版) 題型:選擇題
反應C(s)+H2O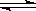 CO(g)+H2(
CO(g)+H2( g)△H>0,達到平衡時,下列說法正確的是( )
g)△H>0,達到平衡時,下列說法正確的是( )
A.加入催化劑,平衡常數不變 B.減小容器體積,正、逆反應速率均減小
C.增大C的量,H2O的轉化率增大 D.升高溫度,平衡向逆反應方向移動
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上月考一化學試卷(解析版) 題型:填空題
硫酸生產中,SO2催化氧化生成SO3:2SO2(g)+O2(g) 2SO3(g)△H<0
2SO3(g)△H<0
(1)如果2min內SO2的 濃度由6mol/L下降為2mol/L,那么,用O2濃度變化來表示的反應速率為 .
濃度由6mol/L下降為2mol/L,那么,用O2濃度變化來表示的反應速率為 .
(2)某溫度下,SO2的平衡轉化率(α)與體系總壓強(p)的關系如圖1所示.根據圖示回答下列問題:
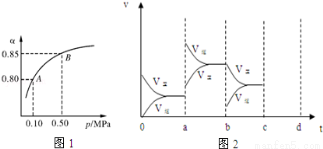
平衡狀態由A變到B時平衡常數K(A) K(B)(填“>”、“<”或“=”).
(3)此反應在恒溫密閉的裝置中進行,能充分說明此反應已達到平衡的標志是 (填字母).
A.接觸室中氣體的平均相對分子質量不再改變
B.接觸室中SO2、O2、SO3的濃度相同
C.接觸室中SO2、SO3的物質的量之比為2:1:2
D.接觸室中壓強不隨時間變化而變化
(4)圖2表示該反應在密閉容器中達到平衡時,由于條件改變而引起反應速度和化學平衡的變化情況,a~ b過程中改變的條件可能是 ;b~c過程中改變的條件可能是 ; 若增大壓強時,請把反應速率變化情況畫在c~d處.
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上月考一化學試卷(解析版) 題型:選擇題
硫代硫酸鈉溶液與稀硫酸反應的化學方程式為Na2S2O3 + H2SO4 = Na2SO4 + SO2↑ +S↓ + H2O,下列各組實驗中最先出現渾濁的是
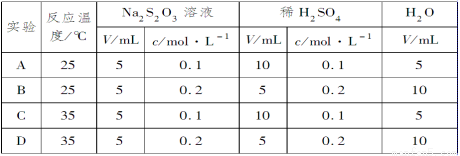
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 物質 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 難溶 | 難溶 | 易溶 |
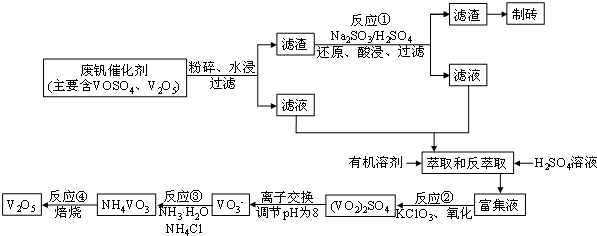
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com