
【題目】(1)把一塊純凈的鋅片插入盛有稀硫酸的燒杯里,可觀察到鋅片逐漸溶解,并有氣體產生;再平行地插入一塊銅片(如圖甲所示),可觀察到銅片上____(填“有”或“沒有”)氣泡產生;再用導線把鋅片和銅片連接起來(如圖乙所示),可觀察到銅片上____(填“有”或“沒有”)氣泡產生。
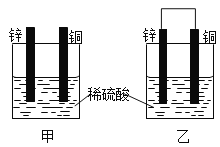
(2)圖乙是一個將_____能轉化為 _____能的裝置,人們把它叫做原電池。外電路中的電子是從_____電極流向______電極。
(3)圖乙中的電極反應式:鋅片________;銅片______。
【答案】沒有 有 化學 電 鋅 銅 Zn - 2e- = Zn 2+ 2 H++ 2e- = H2↑
【解析】
(1)由于金屬活動性順序表中銅排在氫后面,所以銅不和稀硫酸反應;在原電池中,產生氣泡的極只能是正極;
(2)原電池是將化學能轉化為電能的裝置;原電池中電子從負極出發經過外電路到達正極;
(3)鋅比銅活潑,鋅為負極,被氧化,發生Zn-2e-═Zn2+,銅為正極,發生還原反應,電極方程式為2H++2e-═H2↑。
(1)將銅插到硫酸中,金屬銅不能和酸反應置換出氫氣,再用導線把鋅片和銅片連接起來,會形成Zn、Cu、硫酸原電池,在正極上氫離子得電子產生氫氣;
答案:沒有 有
(2)圖乙用導線把鋅片和銅片連接起來,與電解質溶液形成閉合回路,即形成了原電池,原電池是將化學能轉化為電能的裝置;活潑金屬鋅為負極失電子,銅為正極,溶液中氫離子得電子,電子從負極(鋅)出發經過外電路到達正極(銅);
答案:化學 電能 鋅 銅
(3)Zn、Cu、硫酸原電池中,活潑金屬鋅做負極,電極反應為:Zn-2e-=Zn2+,金屬銅做正極,電極反應為:2H++2e-=H2↑;
答案:Zn - 2e- = Zn 2+ 2 H+ + 2e- = H2↑


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】環扁桃酯是用于治療心腦血管疾病的重要化合物,它的一種合成路線如下。

已知:
①
②如下有機物分子結構不穩定,會發生變化:
(1)A的結構簡式是_______________________。
(2)B的結構簡式是_______________________。
(3)F的分子式為C8H6Cl2O。
① E的結構簡式是_______________________。
② E→F的反應類型是____________________。
(4)X的結構簡式是______________________。
(5)試劑a是____________________________。
(6)生成環扁桃酯的化學方程式是_____________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列屬于油脂的用途的是
①人類的營養物質 ②制取肥皂 ③制取甘油 ④制備高級脂肪酸 ⑤制備汽油
A.①②③⑤B.②③④⑤C.①③④⑤D.①②③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至過量。經測定,加入的NaOH的物質的量(mol)和所得沉淀的物質的量(mol)的關系如下圖所示。

(1)寫出代表各線段發生的反應的離子方程式:
OD段________________________________________________,
DC段________________________________________________。
(2)原溶液中Mg2+、Al3+的物質的量濃度之比為________。
(3)圖中C點表示當加入______mol NaOH時,Al3+已經轉化為_____,Mg2+已經轉化為______。
(4)圖中線段OA∶AB=________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中正確的是( )
A.含有碳、氫、氧三種元素的化合物一定是有機物
B.有機物都難溶于水,都是非電解質
C.烴是含有碳元素和氫元素的化合物
D.甲烷是最簡單的烴類有機物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】當有人出現水楊酸反應(頭痛、眩暈、惡心、耳鳴)時,醫生可采取在靜脈中注射下列( )
A.1.25%的NH4Cl溶液B.0.9%的NaHCO3溶液
C.70%的酒精D.10%的鏈霉素
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數值。下列有關敘述正確的是
A. 1.2g鎂在足量的空氣中燃燒生成MgO和Mg3N2,轉移的電子數為0.1NA
B. 將1molCl2通入水中,HClO、Cl-、ClO-粒子數之和為2NA
C. 25℃、101kPa條件下,11.2L丁烷中含極性共價鍵的數目大于5NA
D. CH3+、-OH、NH3各1mol,所含的電子數均為10NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向容積為2 L的密閉容器中充人2 mol A氣體和1 mol B氣體,在一定條件下發生如下反應:2A(g)+B(g) ![]() 3C(g);經2 s后達到平衡,測得C氣體的濃度為0.6 mol·L-1。下列說法中正確的是
3C(g);經2 s后達到平衡,測得C氣體的濃度為0.6 mol·L-1。下列說法中正確的是
①用物質A表示該反應的平均反應速率為0.2 mol·L-1·s-1
②用物質B表示該反應的平均反應速率為0.2 mol·L-1·s-1
③平衡時物質A與B的轉化率相等
④平衡時物質B的濃度為0.2 mol·L-1
A. ①②③ B. ①③ C. ②④ D. ①④
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com