
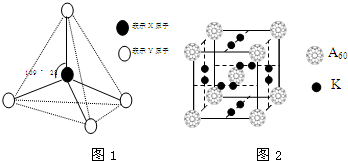
 現有A、B、C、D、E、F六種物質或粒子,其中A、B、C、D都具有如圖1所示的結構或結構單元,(圖中正四面體以外可能有的部分未畫出,虛線不表示化學鍵或分子間作用力,X、Y可以相同也可以不同).A、B的晶體類型相同.工業上利用單質A的同素異形體能與B物質發生置換反應,制取單質G的粗產品.C、D、E、F含有相等的電子數,且D是陽離子,D與F的組成元素相同.C、E、F的晶體類型相同,由E構成的物質常溫下呈液態.
現有A、B、C、D、E、F六種物質或粒子,其中A、B、C、D都具有如圖1所示的結構或結構單元,(圖中正四面體以外可能有的部分未畫出,虛線不表示化學鍵或分子間作用力,X、Y可以相同也可以不同).A、B的晶體類型相同.工業上利用單質A的同素異形體能與B物質發生置換反應,制取單質G的粗產品.C、D、E、F含有相等的電子數,且D是陽離子,D與F的組成元素相同.C、E、F的晶體類型相同,由E構成的物質常溫下呈液態.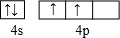 .
.分析 A、B、C、D、E、F六種物質或粒子,其中A、B、C、D都具有正四面體結構或結構單元,D是陽離子,故D為NH4+;C、D、E、F含有相等的電子數,故電子數為10,D與F的組成元素相同,故F為NH3;由E構成的物質常溫下呈液態,故E為H2O;C、E、F的晶體類型相同,屬于分子晶體,故C為CH4;A、B的晶體類型相同,單質A的同素異形體能與B物質發生置換反應,A為金剛石,B為二氧化硅,G為Si.
解答 解:A、B、C、D、E、F六種物質或粒子,其中A、B、C、D都具有正四面體結構或結構單元,D是陽離子,故D為NH4+;C、D、E、F含有相等的電子數,故電子數為10,D與F的組成元素相同,故F為NH3;由E構成的物質常溫下呈液態,故E為H2O;C、E、F的晶體類型相同,屬于分子晶體,故C為CH4;A、B的晶體類型相同,單質A的同素異形體能與B物質發生置換反應,A為金剛石,B為二氧化硅,G為Si.
(1)與A同主族的第四周期元素處于第四周期IVA族,基態原子的價電子排布圖為 ,故答案為:
,故答案為: ;
;
(2)D為NH4+,中心原子J為N,中N原子價層電子對數為4,雜化類型為sp3雜化,F為NH3,易溶于原因是氨分子與水分子間形成氫鍵,
故答案為:sp3;氨分子與水分子間形成氫鍵;
(3)晶胞中C60分子數目為8×$\frac{1}{8}$+1=2,K原子數目為2×6×$\frac{1}{2}$=6,故化學式為:K3C60,
同一周期,從左到右,電負性逐漸增大,同一主族,從上到下,電負性逐漸減小,因此,原子電負性由大到小的順序是:N>C>Si,
每個硅形成的這3個鍵中,必然有1個雙鍵,這樣每個硅原子最外層才滿足8電子穩定結構.顯然,雙鍵數應該是Si原子數的一半,而每個雙鍵有1個π鍵,顯然π鍵數目為30,則1mol G60分子中π鍵的數目為 1.806×1025,
故答案為:K3C60;N>C>Si;1.806×1025;
(4)上述A-F這六種物質或粒子的組成元素中處于同一周期的三種元素為C、N、O,同周期隨原子序數增大,越大第一電離能呈增大趨勢,氮元素2p能級為半滿穩定狀態,第一電離能高于同周期相鄰元素的,故這三種元素第一電離能由大到小的順序:N>O>C,
故答案為:N>O>C;
(5)CoCl3•5F•H2O中的中心離子鈷離子在基態時核外電子排布式為1s22s22p63s23p63d44s2,CoCl3•5NH3•H2O水溶液加AgNO3于該化合物溶液中,有AgCl沉淀生成,說明外界離子有Cl-,過濾后再加AgNO3溶液于濾液中無變化,但加熱至沸騰有AgCl沉淀生成,說明配體中含有Cl-,且其質量為第一次沉淀量的二分之一,說明外界離子有Cl-與配體Cl-之比為2:1,該配離子化學式可能為[CoCl(NH3)5]Cl2•H2O,
故答案為:1s22s22p63s23p63d44s2;[CoCl(NH3)5]Cl2•H2O.
點評 本題是對物質結構與性質的考查,涉及微粒推斷、核外電子排布、配合物、晶胞計算等,利用均攤法進行晶胞有關計算,理解配合物中內界與外界性質的不同,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 需要用托盤天平稱量NaOH固體的質量為1.92g | |
| B. | 將NaOH固體在小燒杯中加水溶解后立即倒入容量瓶中并進行定容 | |
| C. | 在容量瓶中定容時俯視容量瓶刻度線會使溶液濃度偏高 | |
| D. | 定容后塞上瓶塞反復搖勻,靜置后,液面不到刻度線,再加水至刻度線 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
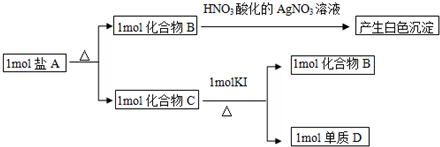
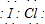 ,該化合物中顯正價的是I元素.
,該化合物中顯正價的是I元素.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H${\;}_{2}^{18}$O中投入Na2O2固體:2H${\;}_{2}^{18}$O+2O${\;}_{2}^{2-}$═4OH-+18O2↑ | |
| B. | 向0.1 mol•L-1、pH=1的NaHA溶液中加入NaOH溶液:H++OH-═H2O | |
| C. | 以金屬銀為陽極電解飽和硫酸銅溶液:Cu2++2H2O═2Cu+O2↑+4H+ | |
| D. | NH4Al(SO4)2溶液中加入Ba(OH)2溶液SO42-使完全沉淀:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
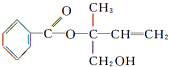
| A. | X的分子式為C12H16O3 | |
| B. | 可用酸性高錳酸鉀溶液區分苯和X | |
| C. | 若單鍵可以旋轉,有機物X中一定在同一平面上的碳原子數為8 | |
| D. | 在Ni作催化劑的條件下,1 mol X最多只能與1 mol H2加成 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 N、P、As、Ga、Cr等元素化合物種類繁多,具有重要的研究價值和應用價值.請回答下列問題:
N、P、As、Ga、Cr等元素化合物種類繁多,具有重要的研究價值和應用價值.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯氣通入水中 Cl2+H2O?H++Cl-+HClO | |
| B. | 甲烷的完全燃燒CH4(g)+2O2(g)$\frac{\underline{\;點燃\;}}{\;}$ CO2(g)+2H2O(l)△H<0 | |
| C. | 冰醋酸加入水中CH3COOH+H2O?CH3COO-+H3O+ | |
| D. | 鐵與水蒸氣反應 2Fe+3H2O$\frac{\underline{\;高溫\;}}{\;}$ Fe2O3+3H2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 12種 | B. | 11種 | C. | 9種 | D. | 7種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,0.1 mol碳酸鈉晶體中含有CO32-的個數為0.1NA | |
| B. | 標準狀況下22.4 L H2O所含分子數為NA | |
| C. | 1 L 0.5 mol•L-1 CH3COOH溶液中,CH3COO-的個數為0.5NA | |
| D. | 在NO、NO2的混合氣體22.4 L中,含有的氮原子數為NA個 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com