

 .
. 分析 Cl2+2NaOH═NaCl+NaClO+H2O中,只有Cl元素的化合價變化,Cl元素的化合價由0升高為+1價,由0降低為-1價;
2H2+O2$\frac{\underline{\;點燃\;}}{\;}$2H2O中,H元素的化合價由0升高為+1價,O元素的化合價由0降低為-2價,以此來解答.
解答 解:Cl2+2NaOH═NaCl+NaClO+H2O中,只有Cl元素的化合價變化,Cl元素的化合價由0升高為+1價,由0降低為-1價,該反應中Cl既被氧化也被還原,該反應中轉移電子為e-,則雙線橋標得失電子數方法為 ;
;
2H2+O2$\frac{\underline{\;點燃\;}}{\;}$2H2O中,H元素的化合價由0升高為+1價,失去電子被氧化;O元素的化合價由0降低為-2價,得到電子被還原,該反應轉移4e-,則雙線橋標得失電子數方法為 ,
,
故答案為: ;
; .
.
點評 本題考查氧化還原反應中轉移電子數目,為高頻考點,把握元素化合價變化及雙線橋法表示轉移電子的方向和數目為解答的關鍵,側重分析與應用能力的考查,題目難度不大.


科目:高中化學 來源: 題型:解答題
 CH3COOC2H5+H2O,該反應的反應類型為取代或酯化反應.
CH3COOC2H5+H2O,該反應的反應類型為取代或酯化反應.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
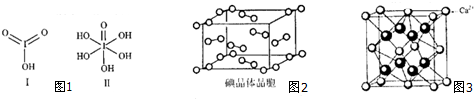
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 常溫下,1.8g H2O含有0.2nA個H-O共價鍵 | |
| B. | 1L 0.3 mol•L-1的FeCl3溶液中Fe3+數目為0.3nA | |
| C. | 標準狀況下,22.4L CCl4中含 nA個CCl4分子 | |
| D. | 標準狀況下,22.4L NO2和CO2的混合氣體含有2nA個氧原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 化學鍵 | H-H | N-H | N≡N |
| 鍵能/kJ•mol-1 | 436 | 391 | 945 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
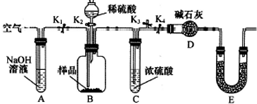 某研究性學習小組對Cu與H2SO4反應的產物種類和性質進行探究.
某研究性學習小組對Cu與H2SO4反應的產物種類和性質進行探究.硫酸/mol•L-1 | 黑色物質出現的溫度/°C | 黑色物質消失的溫度/°C |
| 15 | 約150 | 約236 |
| 16 | 約140 | 約250 |
| 18 | 約120 | 不消失 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使用催化劑是為了加快反應速率,提高生產效率 | |
| B. | 升高溫度可加快逆反應速率但不能改變正反應速率 | |
| C. | 一定條件下,SO2可100%轉化為SO3 | |
| D. | 任何條件下,反應達到平衡,SO2的濃度一定等于SO3的濃度 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH2=CH2 | B. | CH3CH=CH2 | C. | CH3CH3 | D. | CH3CH2CH=CH2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙酸和甲酸甲酯 | B. | 乙烯和環己烷 | C. | 甲醛和果糖 | D. | 淀粉和纖維素 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com