
| 實驗編號 | NaOH溶液的濃度(mol•L-1) | 滴定完成時,NaOH溶液滴入的體積(mL) | 待測鹽酸的體積(mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
分析 (1)依據m=CVM計算需要溶質的質量;
(2)①酚酞遇到堿顯紅色,當最后一滴NaOH溶液加入,溶液由無色恰好變成淺紅色且半分鐘內不褪色,可判斷達到終點;
②先判斷數據的合理性,求出標準NaOH溶液體積,然后依據c(待測)=$\frac{c(標準)×V(標準)}{V(待測)}$求出即可;
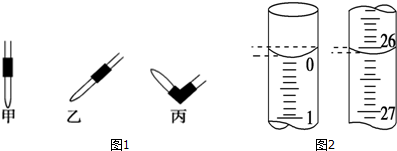
③堿式滴定管的氣泡通常橡皮管內,只要將滴定玻璃頭朝上,并擠橡皮管中的玻璃珠就可以將氣泡沖排出;
④讀取滴定管數值時,應平視刻度線,凹液面最低處與刻度線相切,精確度為0.01mL;
⑤根據c(待測)=$\frac{c(標準)×V(標準)}{V(待測)}$分析不當操作對V(標準)的影響,以此判斷濃度的誤差.
解答 解:(1)配制100mL 0.10mol•L-1 NaOH標準溶液,需要氫氧化鈉質量m=0.10mol/L×0.1L×40g/mol=0.4g;
故答案為:0.4;
(2)①滴定時,當溶液顏色變化且半分鐘內不變色,可說明達到滴定終點,即酚酞在酸中為無色,在堿性溶液中顯淺紅色,
故答案為:最后一滴NaOH溶液加入,溶液由無色恰好變成淺紅色且半分鐘內不褪色;
②3組數據均合理,得出V(標準)=$\frac{22.62+22.72+22.80}{3}$=22.7mL,c(待測)=$\frac{c(標準)×V(標準)}{V(待測)}$=$\frac{0.10mol•{L}^{-1}×22.7mL}{20.00mL}$═0.1135≈0.11mol/L;
故答案為:0.11mol/L;
③堿式滴定管的氣泡通常橡皮管內,只要將滴定玻璃頭朝上,并擠橡皮管中的玻璃珠就可以將氣泡沖排出,故答案為:丙;
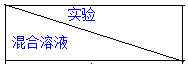
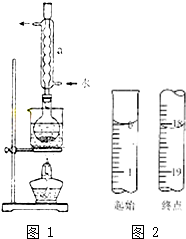
④若滴定開始和結束時,堿式滴定管中的液面如圖2所示,則起始讀數為 0.00 mL,終點讀數為 26.10mL;所用NaOH溶液的體積為 26.10mL;
故答案為:0.00;26.10; 26.10;
⑤A.滴定終點讀數時俯視讀,造成V(標準)偏小,根據c(待測)=$\frac{c(標準)×V(標準)}{V(待測)}$分析,可知c(待測)偏小,故A錯誤;
B.酸式滴定管使用前,水洗后未用待測鹽酸潤洗,待測液的物質的量偏小,造成V(標準)偏小,根據c(待測)=$\frac{c(標準)×V(標準)}{V(待測)}$分析,可知c(待測)偏小,故B錯誤;
C.錐形瓶水洗后未干燥,待測液的物質的量不變,對V(標準)無影響,根據c(待測)=$\frac{c(標準)×V(標準)}{V(待測)}$分析,可知c(待測)不變,故C錯誤;
D.相同質量氫氧化鈉、碳酸鈉,氫氧化鈉消耗鹽酸的物質的量多,所以稱量NaOH固體中混有Na2CO3固體,導致消耗標準液體積偏大,根據c(待測)=$\frac{c(標準)×V(標準)}{V(待測)}$分析,可知C(待測)偏大,故D正確;
E.堿式滴定管尖嘴部分有氣泡,滴定后消失,導致計算時消耗標準液體積偏大,則根據c(待測)=$\frac{c(標準)×V(標準)}{V(待測)}$分析,可知C(待測)偏大,故E正確;
故選:DE.
點評 本題考查了中和滴定實驗,明確使用原理及操作步驟是解題關鍵,注意依據c(待測)=$\frac{c(標準)×V(標準)}{V(待測)}$進行誤差分析的方法,題目難度不大.


 期末寶典單元檢測分類復習卷系列答案
期末寶典單元檢測分類復習卷系列答案科目:高中化學 來源: 題型:實驗題
 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 飽和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
| 壓強(kPa) | 200 | 500 | 1 000 |
| B的濃度(mol•L-1) | 0.04 | 0.1 | 0.27 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.03mol•L-1的蔗糖溶液 | B. | 0.03mol•L-1的BaCl2溶液 | ||
| C. | 0.04mol•L-1的NaCl溶液 | D. | 0.02mol•L-1的CH3COOH溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
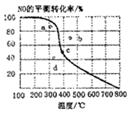 如圖中曲線為一定壓強下NO的平衡轉化率與溫度的關系,圖中a、b、c、d四點表示不同溫度、壓強下2NO(g)+O2(g)?2NO2(g)達到平衡時NO的轉化率,則壓強最大的點為( )
如圖中曲線為一定壓強下NO的平衡轉化率與溫度的關系,圖中a、b、c、d四點表示不同溫度、壓強下2NO(g)+O2(g)?2NO2(g)達到平衡時NO的轉化率,則壓強最大的點為( )| A. | a | B. | b | C. | c | D. | d |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
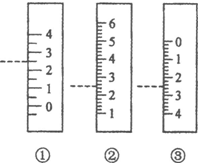 以下是我校化學興趣小組的同學測定廚房食醋中醋酸濃度的實驗,請你參與并完成相關實驗:
以下是我校化學興趣小組的同學測定廚房食醋中醋酸濃度的實驗,請你參與并完成相關實驗:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 Na2S2O3是重要的化工原料,易溶于水.在中性或堿性環境中穩定.
Na2S2O3是重要的化工原料,易溶于水.在中性或堿性環境中穩定.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使用滴定管時,滴定管必須用待裝液潤洗2~3次 | |
| B. | 酸式滴定管不能盛裝堿液,堿式滴定管不能盛裝酸液 | |
| C. | 盛放準確量取待測液的錐形瓶應預先用待測液潤洗 | |
| D. | 滴定操作應重復2至3次,并求出滴定用去的溶液體積的平均值,計算出待測液的濃度 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 人工腎臟可用間接電化學方法除去代謝產物中的尿素[CO(NH2)2],原理如圖.下列有關說法正確的是( )
人工腎臟可用間接電化學方法除去代謝產物中的尿素[CO(NH2)2],原理如圖.下列有關說法正確的是( )| A. | A為電源的負極 | |
| B. | 電解結束后,陰極室溶液的pH與電解前相比將不變 | |
| C. | 陽極室中發生的電極反應為2H++2e-═H2↑ | |
| D. | 若兩極共收集到氣體13.44 L(標準狀況),則除去的尿素為18g(忽略氣體的溶解) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com