
 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 飽和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
| 壓強(kPa) | 200 | 500 | 1 000 |
| B的濃度(mol•L-1) | 0.04 | 0.1 | 0.27 |
分析 (1)①為保證實驗有對比性,只能逐漸改變一個變量分析,CuSO4溶液體積逐漸增多,故H2SO4的量應相等均為30mL,水的量減小,但每組實驗中CuSO4與水的體積之和應相等;
②鋅與硫酸反應使鋅的表面凹凸不平,有很多細小的鋅的顆粒,由于顆粒很小,光被完全吸收,所以看到的固體是灰黑色;Zn能夠置換出Cu,出現紫紅色;
③生成的單質Cu會沉積在Zn的表面,影響了反應速率;
(2)①壓強從 200kPa 增加到500kPa,增大了2.5倍,B的濃度從0.04mol/L增大到0.1mol/L,也增大了2.5倍,說明a=b+c,改變壓強平衡不移動;
②壓強增大的倍數為1000kPa/500kPa=2,B的濃度增大的倍數為0.27mol/L/0.1mol/L=2.7,濃度增大的倍數大于壓強增大的倍數,所以平衡向“正向”移動.
解答 解:(1)①要對比試驗效果,那么除了反應的物質的量不一樣以外,要保證其它條件相同,而且是探究硫酸銅量的影響,那么每組硫酸的量要保持相同,六組反應的總體積也應該相同.A組中硫酸為30ml,那么其它組硫酸量也都為30ml.而硫酸銅溶液和水的總量應相同,F組中硫酸銅20ml,水為0,那么總量為20ml,所以V6=10ml,V9=17.5ml,V1=30ml.
故答案為:30;10;17.5;
②A中沒有加入硫酸銅,鋅與稀硫酸反應后,鋅的表面凹凸不平,有很多細小的鋅的顆粒,由于顆粒很小,光被完全吸收,所以看到的固體是灰黑色;Zn能夠置換出Cu附著在Zn表面,金屬變為紫紅色,
故答案為:灰黑;紫紅;
③因為鋅會先與硫酸銅反應,直至硫酸銅反應完才與硫酸反應生成氫氣,硫酸銅量較多時,反應時間較長,而且生成的銅會附著在鋅片上,會阻礙鋅片與硫酸繼續反應,氫氣生成速率下降,
故答案為:當加入一定量的硫酸銅后,生成的單質銅會沉積在鋅的表面,降低了鋅與溶液的接觸面積.
(2)①根據表中數據,壓強從 200kPa增加到500kPa,增大了2.5倍,B的濃度從0.04mol/L增大到0.1mol/L,也增大了2.5倍,說明濃度增大的倍數和壓強增大的倍數相同,化學計量數滿足a=b+c,改變壓強化學平衡不移動,
故答案為:不;濃度增大的倍數和壓強增大的倍數相同;
②利用表中數據可知,壓強增大的倍數為1000kPa/500kPa=2,B的濃度增大的倍數為0.27mol/L/0.1mol/L=2.7,濃度增大的倍數大于壓強增大的倍數,說明加壓至1000kPa時,C物質變成了非氣態物質,所以增大壓強化學平衡向“正向”移動,
故答案為:正向;加壓至1000kPa時,C物質變成了非氣態物質.
點評 本題考查了影響化學反應速率、化學平衡狀態的影響因素,并且融合了化學實驗,形式新穎靈活,關鍵是分析題中表格的數據,得出正確結論,充分考查了學生的分析、理解能力,是一道不錯的題目,本題難度中等.


 天天練口算系列答案
天天練口算系列答案科目:高中化學 來源: 題型:實驗題
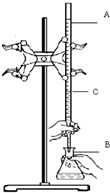 在實驗室用已知濃度的鹽酸滴定某未知濃度的NaOH溶液,裝置和操作如右圖所示.請回答:
在實驗室用已知濃度的鹽酸滴定某未知濃度的NaOH溶液,裝置和操作如右圖所示.請回答:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向鹽酸中滴加氨水:H++OH-═H2O | |
| B. | Fe(OH)3溶于氫碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 銅溶于稀硝酸:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| D. | Na2O2與H2O反應制備O2:Na2O2+H2O═2Na++2OH-+O2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溶解、過濾、蒸發 | B. | 溶解、過濾、洗滌、干燥 | ||
| C. | 溶解、過濾、結晶 | D. | 溶解、結晶、干燥 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將含硫酸的廢液倒入水槽,用水沖入下水道 | |
| B. | 對醫用酒精進行蒸餾操作可得到更高純度的酒精溶液 | |
| C. | 加熱高錳酸鉀固體制取并收集氧氣結束后,應立即停止加熱 | |
| D. | 蒸餾實驗時,冷水應從上口進下口出 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | BaSO4難溶于水,所以BaSO4是非電解質 | |
| B. | 弱電解質的導電性一定比強電解質弱 | |
| C. | 25℃時0.1mol/L的CH3COOH溶液pH=3,說明CH3COOH為弱電解質 | |
| D. | 某物質能導電,所以該物質一定是電解質 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 瓦斯中甲烷和氧氣的質量比為1:4時極易爆炸,此時甲烷與氧氣的體積比為1:2 | |
| B. | 欲配制1.00 L1.00 mol•L-1的NaCl溶液,可將58.5 g NaCl溶于1.00 L水中 | |
| C. | 22.4LN2和H2的混合氣體中含NA個原子 | |
| D. | 3mol單質Fe完全轉變為Fe3O4,得到8NA個電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗編號 | NaOH溶液的濃度(mol•L-1) | 滴定完成時,NaOH溶液滴入的體積(mL) | 待測鹽酸的體積(mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com