
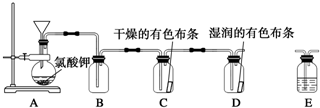
分析 (1)裝置中反應試劑是濃鹽酸易揮發,需要用分液漏斗加入;
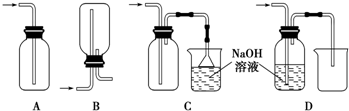
(2)氯氣密度大于空氣密度,能夠溶于水,易于氫氧化鈉溶液反應;
(3)制備出的氯氣含有揮發出的氯化氫,通過飽和食鹽水可以除去,減小氯氣的溶解性;探究使有色布條褪色的是氯氣還是氯氣與水反應的生成物,需要在整套裝置中添加裝置E,其中加入濃硫酸,應在C裝置前干燥氯氣;
(4)鐵在氯氣中燃燒發出棕黃色煙氯化鐵;依據氯化鐵性質分析三價鐵離子結合氫氧根離子會生成紅褐色沉淀,和鐵反應生成氯化亞鐵,溶液顏色發生改變,溶解后加入硫氰酸鉀溶液呈血紅色檢驗;
(5)氯氣有毒,直接排放能夠引起空氣污染,氯氣與氫氧化鈉溶液反應,可以用氫氧化鈉溶液吸收.
解答 解:(1)裝置中反應試劑是濃鹽酸易揮發,需要用分液漏斗加入,改長頸漏斗為分液漏斗,故答案:改長頸漏斗為分液漏斗;
(2)氯氣密度大于空氣密度,能夠溶于水,易于氫氧化鈉溶液反應;
A.沒有出去空氣,集氣瓶容易發生爆炸,故A錯誤;
B.氯氣密度大于空氣密度,應選擇向上排空氣法收集,故B錯誤;
C.氯氣密度大于空氣密度,選擇向上排空氣法收集,氯氣有毒用氫氧化鈉吸收,應用防止倒吸裝置,故C正確;
D.氯氣與氫氧化鈉溶液反應,收集不到氯氣,故D錯誤;
故選:C;
(3)制備出的氯氣含有揮發出的氯化氫,通過飽和食鹽水可以除去,減小氯氣的溶解性;探究使有色布條褪色的是氯氣還是氯氣與水反應的生成物,需要在整套裝置中添加裝置E,其中加入濃硫酸,應在C裝置前干燥氯氣,選擇裝置B、C之間;
故答案為:飽和食鹽水;b;
(4)鐵在氯氣中燃燒,集氣瓶內和瓶口出現棕黃色煙氯化鐵;依據氯化鐵性質分析三價鐵離子結合氫氧根離子會生成紅褐色沉淀,和鐵反應生成氯化亞鐵,溶液顏色發生改變,溶解后加入硫氰酸鉀溶液呈血紅色檢驗;
a.氯水,加入不出現明顯現象,不能檢驗鐵離子存在,故a不選;
b.蒸餾水和鐵粉,用蒸餾水溶解氯化鐵的溶液中加入鐵反應溶液顏色變化為淺綠色,證明鐵離子存在,故b正確;
c.蒸餾水和氫氧化鈉溶液,用蒸餾水溶解氯化鐵后加入氫氧化鈉溶液會生成氫氧化鐵紅褐色沉淀,可以鑒別鐵離子的存在,故c正確;
d.蒸餾水和KSCN溶液,用蒸餾水溶解氯化鐵,加入KSCN溶液出現血紅色溶液證明鐵離子存在,故d正確;
故答案為:集氣瓶內和瓶口出現棕黃色煙;bcd;
(5)氯氣有毒,直接排放能夠引起空氣污染,應該在裝置D后增加一個盛裝濃堿液的裝置,使堿液吸收逸出的氯氣尾氣;
故答案為:在裝置D后增加一個盛裝濃堿液的裝置,使堿液吸收逸出的氯氣尾氣.
點評 本題考查了氯氣的制備及性質檢驗,熟悉氯氣制備原理及收集、凈化、尾氣處理裝置的選擇是解題關鍵,題目難度中等.


 同步練習強化拓展系列答案
同步練習強化拓展系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
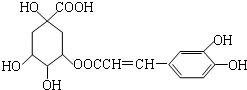
| A. | 分子式為C16H18O9 | |
| B. | 1mol咖啡鞣酸水解時可消耗8molNaOH | |
| C. | 咖啡鞣酸分子中所有原子都在同一平面上 | |
| D. | 與濃溴水既能發生取代反應又能發生加成反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 次氯酸的電子式 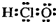 | |
| B. | S2-的結構示意圖: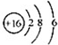 | |
| C. | 質子數為53,中子數為78的碘原子:13153I | |
| D. | NH4I的電子式: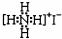 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH4+、Fe2+、NO3-、H+ | B. | K+、Mg2+、I-、ClO- | ||
| C. | K+、Ba2+、Cl-、Br- | D. | K+、HCO3-、Cl-、H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 78% | B. | 22% | C. | 14% | D. | 13% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
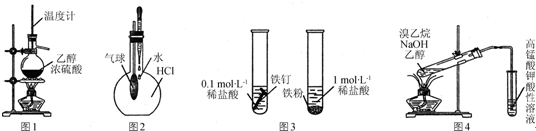
| A. | 用圖1所示裝置制取乙烯 | |
| B. | 用圖2所示方法驗證HCl氣體易溶于水 | |
| C. | 用圖3所示方法探究固體表面積對反應速率的影響 | |
| D. | 用圖4所示方法檢驗溴乙烷與NaOH醇溶液共熱產生乙烯 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com