
對于任何一個化學平衡體系,以下變化或采取的措施,平衡一定發生移動的是( )
①加入一種反應物,②增大體系的壓強,③升高溫度,④使用催化劑,⑤化學平衡常數減小。
A.①②③⑤ B.①②③④⑤ C.③⑤ D.①②③
科目:高中化學 來源:2016屆內蒙古高三上學期期中化學試卷(解析版) 題型:選擇題
下列說法錯誤的是( )
A、二氧化硅用于制備太陽能電池板
B、氯氣可用于自來水殺菌消毒
C、從海水中提取物質不一定必須通過化學反應才能實現
D、氫氟酸不能保存在玻璃瓶中
查看答案和解析>>
科目:高中化學 來源:2016-2017學年浙江省高二上期中化學卷(解析版) 題型:選擇題
下列表述中合理的是
A.在101kPa下,1g物質完全燃燒所放出的熱量叫做該物質的熱值
B.把FeCl3的水溶液加熱蒸干可得到FeCl3固體
C.用25 mL堿式滴定管量取20.00mL高錳酸鉀溶液
D.太陽能電池是把太陽能轉化為內能的裝置
查看答案和解析>>
科目:高中化學 來源:2016-2017學年云南省高二上期中化學卷(解析版) 題型:選擇題
下列說法正確的是( )
A. 在測定中和熱的實驗中, 為了準確測定反應混合溶液的溫度,實驗中溫度計水銀球應與小燒杯底部接觸
B. 酸堿中和滴定實驗中,錐形瓶要用待裝液預先潤洗
C. 在測定中和熱的實驗中,用0.5mol·L-1NaOH溶液分別與0.5 mol·L-1的鹽酸、醋酸溶液反應,如所取的溶液體積相等,則測得的中和熱數值相同
D. 測溶液PH值時,PH試紙不能潤濕
查看答案和解析>>
科目:高中化學 來源:2016-2017學年云南省高二上期中化學卷(解析版) 題型:選擇題
下列說法正確的是( )
A.正反應是放熱反應的可逆反應,升高溫度v(正)>v(逆)
B.加壓可使速率加快,是因為增加活化分子百分數而使反應速率加快
C.活化分子的碰撞不一定都能發生化學反應
D.催化劑可改變反應進程,故加催化劑改變了一個反應的 △H
查看答案和解析>>
科目:高中化學 來源:2017屆寧夏高三上月考四化學試卷(解析版) 題型:填空題
【化學——選修物質結構與性質】
X是第四周期元素,最外層只有1個電子,次外層的所有原子軌道均充滿電子。元素Y基態原子的3p軌道上有2個未成對電子。元素Z 的原子最外層電子數是其內層的3倍。回答下列問題:
(1)元素X在元素周期表中位于 區,單質X的晶體類型為 ,其中X原子的配位數為 。
(2)已知元素Y可與元素Z的相對原子質量只差為16,則元素Y基態原子的外圍電子排布圖為 ,其同周期元素中,第一電離能最大的是________________(寫元素符號)。元素Y的含氧酸中,酸性最強的是_____________(寫化學式),該酸根離子的立體構型為_____________。
(3)Z的氫化物在乙醇中的溶解度大于Y的氫化物,其原因是 。
(4)X的氯化物與氨水反應可形成配合物[X(NH3)4]Cl2,1mol該配合物中含有σ鍵的數目為 。
(5)X與Y形成的一種化合物的立方晶胞如圖所示。
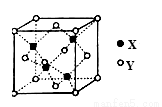
該化合物的化學式為_______________,已知此晶體的密度為ρg·cm–3,阿伏伽德羅常數為NA,則此晶胞中X與Y的最近距離是 cm。(寫出計算式,不要求計算結果。)
查看答案和解析>>
科目:高中化學 來源:2017屆寧夏高三上月考四化學試卷(解析版) 題型:選擇題
下列離子方程式書寫不正確的是
A.碳酸鈉與次氯酸反應:CO32-+2HClO=2ClO-+H2O+CO2↑
B.二氧化硫通入次氯酸鈉溶液中:SO2+ClO-+2OH-=SO42-+Cl-+H2O
C.明礬溶液中加氫氧化鋇溶液至硫酸根恰好沉淀完全:
Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
D.碘化亞鐵溶液與少量氯氣反應:2I-+Cl2=I2+2Cl-
查看答案和解析>>
科目:高中化學 來源:2017屆遼寧省高三上模擬一化學試卷(解析版) 題型:填空題
工業上可以利用廢氣中的CO2為原料制取甲醇。請回答下列問題:
(1) 已知常溫常壓下,下列兩個可逆反應的能量變化如下圖所示:
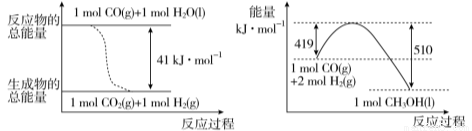
請寫出左圖反應的平衡常數表達式K= 。
請寫出由二氧化碳和氫氣制備甲醇的熱化學方程式 。
(2) 如果只改變一個條件使上述反應方程式的平衡常數K值變大,則該反應________(選填編號)。
A.一定向正反應方向移動 B.在平衡移動時,正反應速率先增大后減小
C.一定向逆反應方向移動 D.在平衡移動時,逆反應速率先減小后增大
(3) 在其他條件不變的情況下,將容器體積壓縮到原來的1/2,與原平衡相比,下列有關說法正確的是________(填字母)。
A.H2的濃度減小 B.正反應速率加快,逆反應速率也加快
C.甲醇的物質的量增加 D.重新平衡時,n(H2)/n(CH3OH)增大
(4) 保持溫度和體積不變,通入1molCO2和3molH2 ,下列能說明該反應已達平衡狀態的是________(填字母)。
,下列能說明該反應已達平衡狀態的是________(填字母)。
A.n(CO2)∶n(H2)∶n(CH3OH)∶n(H2O)=1∶3∶1∶1
B.容器內壓強保持不變
C.H2的消耗速率與CO2的消耗速率之比為3∶1
D.容器內氣體的平均相對分子質量保持不變
(5) 若反應容器的容積為2.0 L,反應時間4.0 min,容器 內氣體的密度減少了2.0 g·L-1。在這段時間內CO2的平均反應速率為_______________
內氣體的密度減少了2.0 g·L-1。在這段時間內CO2的平均反應速率為_______________
(6) 有人設計甲醇-空氣燃料電池電源, 用石墨作電極電解200 mL含有下列離子的溶液:
用石墨作電極電解200 mL含有下列離子的溶液:
離子 | Cu2+ | H+ | Cl- | SO |
c/(mol·L-1) | 0.5 | 2 | 2 | 0.5 |
電解一段時間后,標況下當兩極收集到相同體積的氣體時,陽極上收集到氧氣的質量為____________(忽略溶液體積的變化及電極產物可能存在的溶解現象)。也有人用此電源利用電解法制備Na2FeO4,陽極材料為鐵,其電解質溶液用NaOH溶液,陽極反應式為 。
查看答案和解析>>
科目:高中化學 來源:2017屆江西師大附中高三上學期期中化學試卷(解析版) 題型:選擇題
下列敘述Ⅰ和Ⅱ均正確并有因果關系的是( )
選項 | 敘述Ⅰ | 敘述Ⅱ |
A | 1?己醇的沸點比己烷的沸點高 | 1?己醇和己烷可通過蒸餾初步分離 |
B | 原電池可將化學能轉化為電能 | 原電池需外接電源才能工作 |
C | 乙二酸可與KMnO4溶液發生反應 | 乙二酸具有酸性 |
D | Na在Cl2中燃燒的生成物含離子鍵 | NaCl固體可導電 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com