

分析 (1)若以方案1加熱NaNO2和NH4Cl的濃溶液制得N2,反應物狀態是固液混合、反應條件是加熱,應該選用固液加熱型裝置;
(2)若按方案2制得干燥、純凈的N2,且需要的NH3以生石灰和濃氨水作原料,先用生石灰和濃氨水混合制取氨氣,然后用堿石灰干燥氨氣,將氨氣和CuO加熱制取氮氣,再用酸吸收未反應的氨氣,最后獲取干燥、純凈的氮氣;在加熱條件下,氨氣和CuO加熱生成Cu和氮氣;
(3)氮氣和空氣相對分子質量接近,所以不宜采用排空氣法收集;可以用塑料袋直接收集;
(4)根據制備方案中氮氣純度分析.在N2純度要求不甚嚴格的情況下,方案2和方案3中Cu 和 CuO 可以循環使用.
解答 解:(1)若以方案1加熱NaNO2和NH4Cl的濃溶液制得N2,反應物狀態是固液混合、反應條件是加熱,應該選用固液加熱型裝置,故選A;
(2)若按方案2制得干燥、純凈的N2,且需要的NH3以生石灰和濃氨水作原料,先用生石灰和濃氨水混合制取氨氣,不需要加熱,應該選取固液混合不加熱型裝置,故選B;然后用堿石灰干燥氨氣,選D;將氨氣和CuO加熱制取氮氣,選B;再用酸吸收未反應的氨氣,選C;最后獲取干燥、純凈的氮氣,所以儀器連接順序是E→D→B→C;在加熱條件下,氨氣和CuO加熱生成Cu和氮氣,反應方程式為2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O,
故答案為:E→D→B→C;2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O;
(3)N2的相對分子質量28與空氣的平均相對分子質量相近,故不宜用排空氣法;可直接用塑料袋收集,
故答案為:N2的相對分子質量28與空氣的平均相對分子質量相近(用氣體密度大小比較回答問題也給分);以塑料袋直接收集;
(4)從制備過程看,方案1和2能得到純凈的氮氣,而方案3制取的氮氣中混有稀有氣體、二氧化碳、水蒸氣等物質,所以方案3氮氣純度最差;方案2和3反應原理簡單,原料來源多,銅和氧化銅可以循環利用;
故答案為:方案3;Cu 和 CuO 可以循環使用,節省藥品.
點評 本題考查氣體制備實驗方案設計,為高頻考點,明確實驗原理及實驗基本操作過程是解本題關鍵,會從實驗原理及實驗步驟方面進行評價,難點是儀器連接順序,題目難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | NaCl溶液中離子的總濃度和NaClO溶液中離子的總濃度相等 | |
| B. | NaCl溶液中離子的總濃度大于NaClO溶液中離子的總濃度 | |
| C. | NaCl溶液中離子的總濃度小于NaClO溶液中離子的總濃度 | |
| D. | NaCl溶液的pH大于NaClO溶液的pH |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
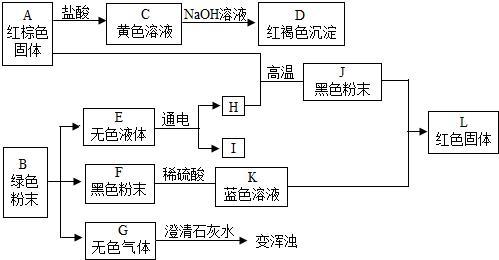
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 l,2二溴乙烷可作汽油抗爆劑的添加劑,常溫下它是無色液體,密度2.189cm-3,沸點131.4℃,熔點9.79℃,不溶于水,易溶于醇、醚、丙酮等有機溶劑.在實驗室中可用下列反應制備1,2二溴乙烷.
l,2二溴乙烷可作汽油抗爆劑的添加劑,常溫下它是無色液體,密度2.189cm-3,沸點131.4℃,熔點9.79℃,不溶于水,易溶于醇、醚、丙酮等有機溶劑.在實驗室中可用下列反應制備1,2二溴乙烷.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 實驗室制備1,2-二溴乙烷的反應原理如下:
實驗室制備1,2-二溴乙烷的反應原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 狀態 | 無色液體 | 無色液體 | 無色液體 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸點/0C | 78.5 | 132 | 34.6 |
| 熔點/0C | -130 | 9 | -116 |
| 溶解性 | 易溶水 | 難溶水 | 微溶于水 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某研究性學習小組為合成1-丁醇,查閱資料得知一條合成路線:
某研究性學習小組為合成1-丁醇,查閱資料得知一條合成路線:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 溴乙烷是一種重要的有機化工原料,其沸點為38.4℃.制備溴乙烷的一種方法是乙醇與氫溴酸反應.某課外小組欲在實驗室制備溴乙烷的裝置如右圖,實驗操怍步驟如下:
溴乙烷是一種重要的有機化工原料,其沸點為38.4℃.制備溴乙烷的一種方法是乙醇與氫溴酸反應.某課外小組欲在實驗室制備溴乙烷的裝置如右圖,實驗操怍步驟如下:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 純水的導電性很差,所以水不是電解質 | |
| B. | SO3水溶液的導電性很好,所以SO3是電解質 | |
| C. | 液態的銅導電性很好,所以銅是電解質 | |
| D. | Na2O液態時能導電,所以Na2O是電解質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 單質:⑥⑦ | B. | 氧化物:②⑨ | C. | 堿:①④ | D. | 有機物:③⑤ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com