
 溶液出現藍色且30s內不褪色
溶液出現藍色且30s內不褪色
分析 (1)由裝置Ⅱ中發生的反應可知,裝置Ⅰ中產生的氣體為SO2,亞硫酸鈉與硫酸反應生成硫酸鈉、二氧化硫與水;
(2)裝置Ⅱ中獲得已析出的晶體,分離固體與液態,應采取過濾操作;
(3)裝置Ⅲ用于處理尾氣,吸收為反應的二氧化硫,應防止倒吸,且不能處于完全密閉環境中;
(4)NaHSO3溶液中HSO3-的電離程度大于水解程度,溶液呈酸性,故檢驗溶液呈酸性即可;
(5)Na2S2O5晶體在空氣中易被氧化為Na2SO4,用鹽酸、氯化鋇溶液檢驗樣品中是否含有硫酸根即可;
(6)①由消耗碘的量,結合SO2+I2+2H2O═H2SO4+2HI計算二氧化硫的質量,進而計算濃度;
②若有部分HI被空氣氧化,則消耗碘的量偏小,故測定二氧化硫的量偏小.
解答 解:(1)由裝置Ⅱ中發生的反應可知,裝置Ⅰ中產生的氣體為SO2,亞硫酸鈉與硫酸反應生成硫酸鈉、二氧化硫與水,反應方程式為:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,
故答案為:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O;
(2)裝置Ⅱ中獲得已析出的晶體,分離固體與液態,應采取過濾進行分離,
故答案為:過濾;
(3)a.裝置應將導管深入氨水中可以吸收二氧化硫,但為密閉環境,裝置內壓強增大易產生安全事故,故錯誤;
b.該裝置吸收二氧化硫能力較差,且為密閉環境,裝置內壓強增大易產生安全事故,故錯誤;
c.該裝置不能吸收二氧化硫,所以無法實現實驗目的,故錯誤;
d.該裝置中氫氧化鈉與二氧化硫反應,可以吸收,且防止倒吸,故正確;
故答案為:d;
(4)NaHSO3溶液中HSO3-的電離程度大于水解程度,溶液呈酸性,測定溶液的pH,可以確定溶液酸堿性,酸性溶液可以使濕潤藍色石蕊試紙變紅,所以能用測定溶液pH值、濕潤的藍色石蕊試液檢驗,而加入Ba(OH)2溶液、HCl溶液、品紅溶液都不能說明溶液呈酸性,故選ae;
故答案為:ae;
(5)Na2S2O5中S元素的化合價為+4價,因此會被氧化為為+6價,即晶體在空氣中易被氧化為Na2SO4,用鹽酸、氯化鋇溶液檢驗樣品中是否含有硫酸根即可,實驗方案為:取少量Na2S2O5晶體于試管中,加入適量水溶解,滴加鹽酸,振蕩,再滴加氯化鋇溶液,有白色沉淀生成,
故答案為:取少量Na2S2O5晶體于試管中,加入適量水溶解,滴加鹽酸,振蕩,再滴加氯化鋇溶液,有白色沉淀生成;
(6)①令100mL葡萄酒中二氧化硫的質量為mg,則:
SO2+2H2O+I2═H2SO4+2HI
64g 1mol
mg 0.025L×0.01mol/L
所以,64g:mg=1mol:0.025L×0.01mol/L,
解得m=0.016
故該次實驗測得樣品中抗氧化劑的殘留量(以游離SO2計算)為$\frac{0.016g}{0.1L}$=0.16 g/L
故答案為:0.16;
②若有部分HI被空氣氧化,則消耗碘的量偏小,故測定二氧化硫的量偏小,則測定結果偏低,
故答案為:偏低.
點評 本題考查物質的制備實驗、實驗方案設計、物質含量的測定、氧化還原反應滴定等,難度中等,明確實驗原理是解本題關鍵,根據物質的性質分析解答,注意元素化合物知識的積累和靈活運用.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
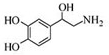
| A. | 每個去甲腎上腺素分子中含有3個酚羥基 | |
| B. | 每個去甲腎上腺素分子中含有1個手性碳原子 | |
| C. | 1mol去甲腎上腺素最多與2mol Br2發生取代反應 | |
| D. | 去甲腎上腺素既能與碳酸氫鈉反應生成二氧化碳氣體,又能與鹽酸反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
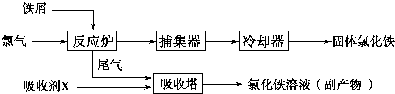
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
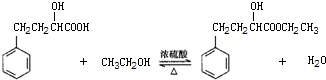
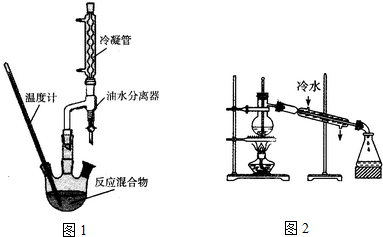
| 相對分子量 | 密度(g/cm3) | 沸點(℃) | 水溶性 | |
| 2-羥基-4-苯基丁酸 | 180 | 1.219 | 357 | 微溶 |
| 乙 醇 | 46 | 0.789 | 78.4 | 易溶 |
| 2-羥基-4-苯基丁酸乙酯 | 208 | 1.075 | 212 | 難溶 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ,B與亞硝酸,在0~5℃反應后生成的產物與溴亞化銅和氰化鉀反應生成C,C與氫氧化鈉溶液共熱生成2-氯-4-硝基苯酚,試推測A、B、C的構造式.
,B與亞硝酸,在0~5℃反應后生成的產物與溴亞化銅和氰化鉀反應生成C,C與氫氧化鈉溶液共熱生成2-氯-4-硝基苯酚,試推測A、B、C的構造式.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 把碳棒放在酒精噴燈上灼燒 2-3min 后即投入到冷水中,重復操作幾次,可制得多孔碳棒 | |
| B. | 在中和熱的測定實驗中,將氫氧化鈉溶液迅速倒入盛有鹽酸的量熱計中,立即讀出并記錄 溶液的起始溫度,充分反應后再讀出并記錄反應體系的最高溫度 | |
| C. | K2CrO4 溶液中存在平衡 2CrO${\;}_{4}^{2-}$+2H+Cr2O${\;}_{7}^{2-}$+H2O,加稀硝酸則溶液由黃色變為橙色 | |
| D. | 分光光度計可以用來測定某些化學反應的反應速率 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com