
| A. | 3.9gNa2O2固體中含有的陰離子數為0.05 NA | |
| B. | 標準狀況下,2.24LCCl4所含原子數為0.5 NA | |
| C. | 1L 0.1mol/L醋酸溶液中含有的CH3COOH分子數為0.1 NA | |
| D. | 56g鐵絲與一定量Cl2發生反應,當鐵粉反應完全時,電子轉移的數目可能為2.2 NA |
分析 A.根據過氧化鈉的物質的量結合一個過氧化鈉化學式中含有的陰離子個數計算總陰離子個數;
B.標準狀況下四氯化碳不是氣體;
C.醋酸是弱電解質存在電離平衡;
D.鐵和氯氣反應生成氯化鐵,56g鐵的物質的量為1mol,與足量氯氣完全反應失去3mol電子;
解答 解:A.一個過氧化鈉化學式中含有1個陰離子,3.9gNa2O2的物質的量=$\frac{3.9g}{78g/mol}$=0.05mol,所以含有的陰離子數是0.05 NA,故A正確;
B.標準狀況下四氯化碳不是氣體,2.24LCCl4所含物質的量不是0.1mol,原子數不是0.5 NA,故B錯誤;
C.1L 0.1mol/L醋酸溶液中,醋酸是弱電解質存在電離平衡,含有的CH3COOH分子數小于0.1 NA ,故C錯誤;
D.56g鐵粉的物質的量為1mol,1mol鐵與足量氯氣完全反應失去3mol電子,轉移電子數目為3NA,故D錯誤;
故選A.
點評 本題考查阿伏加德羅常數的有關計算和判斷,題目難度中等,注意明確標況下氣體摩爾體積的使用條件,要求掌握好以物質的量為中心的各化學量與阿伏加德羅常數的關系,試題有利于培養學生的邏輯推理能力,提高學生靈活運用基礎知識解決實際問題的能力.


 互動英語系列答案
互動英語系列答案科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2H2(g)+O2(g)→2H2O(l)+Q1 2H2(g)+O2(g)→2H2O(g)+Q2 | |
| B. | S(g)+O2(g)→SO2(g)+Q1 S(s)+O2(g)→SO2(g)+Q2 | |
| C. | C(s)+0.5O2(g)→CO(g)+Q1 C(s)+O2(g)→CO2(g)+Q2 | |
| D. | H2(g)+Cl2(g)→2HCl(g)+Q1 $\frac{1}{2}{H_2}$(g)+$\frac{1}{2}C{l_2}$(g)→HCl(g)+Q2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2KClO3(s)═2KCl(s)+3O2(g)△H=-78.03kJ•mol-1 △S=+1110 J•mol-1•K-1 | |
| B. | CO(g)═C(s,石墨)+$\frac{1}{2}$O2(g)△H=+110.5kJ•mol-1△S=-89.36 J•mol-1•K-1 | |
| C. | 4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)△H=-444.3kJ•mol-1△S=-280.1 J.mol-1•K-1 | |
| D. | NH4HCO3(s)+CH3COOH(aq)═CO2(g)+CH3COONH4(aq)+H2O(l)△H=+37.301kJ•mol-1△S=+184.05 J•mol-1•K-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 含有大量Al3+的溶液:Na+、NH4+、SO42-、Cl- | |
| B. | 含有大量OH-的溶液:Na+、Ca2+、SO42-、CO32- | |
| C. | 含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN- | |
| D. | 含有大量NO3-的溶液:H+、Fe2+、SO42-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 含20.0g NaOH的稀溶液與稀鹽酸完全中和,放出28.7kJ的熱量,則稀醋酸和稀NaOH溶液反應的熱化學方程式為:NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l);△H=-57.4kJ•mol-1 | |
| B. | 已知C(石墨,s)=C(金剛石,s);△H>0,則金剛石比石墨穩定 | |
| C. | 已知反應2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ•mol-1,則H2的燃燒熱為571.6kJ•mol-1 | |
| D. | 已知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2,則△H1<△H2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1Ll.00mol•L-1NaCl溶濃中NaCl分子數為NA | |
| B. | 標準狀況下,2.24L由N2和O2組成的混合氣體中所含的原子數為0.1NA | |
| C. | 常溫下,0.1molCl2溶于水時,轉移的電子效是0.1NA | |
| D. | 0.lmolFe與過量稀HNO3反應時,轉移的電子教為0.3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
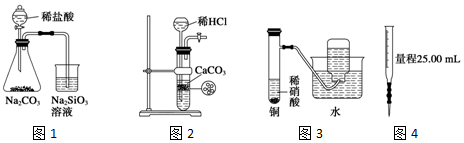
| A. | 圖1為證明非金屬性強弱:Cl>C>Si | |
| B. | 圖2為制備少量CO2并控制反應 | |
| C. | 圖3為制備并收集少量NO氣體 | |
| D. | 圖4量取0.10mol•L-1 KOH溶液20.00mL |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com