
| A. | Y的最高價氧化物的熔點比X的最高價氧化物的熔點低 | |
| B. | 原子半徑:Y>Z>X | |
| C. | Y的最高價氧化物的水化物只能與酸反應,不能與堿反應 | |
| D. | 由Z、Y兩元素分別形成的單質均存在同素異形體 |
分析 短周期元素X、Y、Z的原子序數依次遞增,X、Z同主族,則X處于第二周期、Y處于第三周期,Y原子最外層電子數比X原子次外層電子數多1,則Y原子最外層電子數為3,它們的原子最外層電子數之和為11,則X、Z原子最外層電子數為$\frac{11-3}{2}$=4,可推知X為C元素、Z為Si、Y為Al,據此解答.
解答 解:短周期元素X、Y、Z的原子序數依次遞增,X、Z同主族,則X處于第二周期、Y處于第三周期,Y原子最外層電子數比X原子次外層電子數多1,則Y原子最外層電子數為3,它們的原子最外層電子數之和為11,則X、Z原子最外層電子數為$\frac{11-3}{2}$=4,可推知X為C元素、Z為Si、Y為Al.
A.氧化鋁屬于離子晶體,二氧化碳屬于分子晶體,常溫下為氣體,故氧化鋁的熔點高于二氧化碳的熔點,故A錯誤;
B.同周期自左而右原子半徑減小、同主族自上而下原子半徑增大,故原子半徑Y(Al)>Z(Si)>X(C),故B正確;
C.Y的最高價氧化物的水化物為氫氧化鋁,屬于兩性氫氧化物,能與酸、堿反應,故C錯誤;
D.硅單質存在晶體硅與無定形硅,而鋁單質不存在同素異形體,故D錯誤,
故選B.
點評 本題考查結構性質位置關系綜合應用,推斷元素是解題關鍵,注意微粒半徑比較與元素化合物性質的掌握.


 暑假作業海燕出版社系列答案
暑假作業海燕出版社系列答案 本土教輔贏在暑假高效假期總復習云南科技出版社系列答案
本土教輔贏在暑假高效假期總復習云南科技出版社系列答案 暑假作業北京藝術與科學電子出版社系列答案
暑假作業北京藝術與科學電子出版社系列答案 第三學期贏在暑假系列答案
第三學期贏在暑假系列答案科目:高中化學 來源: 題型:選擇題
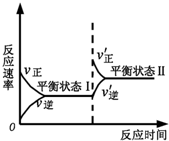
| A. | 反應達平衡時,正反應速率和逆反應速率相等 | |
| B. | 該反應達到平衡狀態Ⅰ后,減小反應物濃度,平衡發生移動,達到平衡狀態Ⅱ | |
| C. | 該反應達到平衡狀態Ⅰ后,增大反應物濃度,平衡發生移動,達到平衡狀態Ⅱ | |
| D. | 同一種反應物在平衡狀態Ⅰ和平衡狀態Ⅱ時濃度不相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,2LpH=12的氨水中含有OH-數目為0.02NA | |
| B. | 氯堿工業中,外電路中轉移電子數為0.3NA時產生氣體體積(標準狀況)為4.48L | |
| C. | 標準狀況下,11.2LCH3Cl中非極性共價鍵數目等于2.0NA | |
| D. | 一定條件下,1molI2和0.2molH2混合充分反應,轉移的電子數為0.4NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 熔點/℃ | 沸點/℃ | 備注 | |
| 白磷 | 44 | 280.5 | |
| PH3 | -133.8 | -87.8 | 難溶于水、有還原性 |
| SiF4 | -90 | -86 | 易水解 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 裝置 | 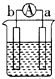 CuSO4溶液 | 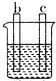 稀硫酸 |  稀硫酸 |
| 現象 | a極質量減小 b極質量增大 | b極有氣泡 c極無明顯現象 | 電流從a極流向d極 |
| A. | d>a>b>c | B. | b>c>d>a | C. | a>b>c>d | D. | a>b>d>c |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一定條件下,將1molN2和3molH2混合,充分反應后轉移的電子數為NA | |
| B. | 1.5molNO2與足量水反應,轉移的電子數為1.5NA | |
| C. | 6.4g由S2、S4、S8組成的混合物含硫原子數為0.2NA | |
| D. | 常溫常壓下,11.2LCl2含氯原子數為NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com