
 工業合成氨與制備硝酸一般可連續生產,流程如圖所示:
工業合成氨與制備硝酸一般可連續生產,流程如圖所示: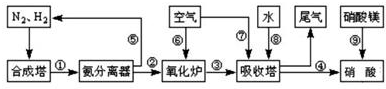
| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
分析 (1)根據平衡常數表達式以及各種物質的濃度知識來回答;
(2)溫度和平衡常數間的關系取決于平衡受溫度的影響情況;
(3)對于放熱反應,溫度升高,則化學平衡向逆向移動;
(4)根據蓋斯定律來計算反應的焓變,進而書寫熱化學方程式;
(5)氨氣在純氧中燃燒,生成氮氣和水,燃料電池中,燃料做負極.
解答 解:(1)根據題意:CO+H2O(g)?CO2 +H2
初始濃度:0.2 0.3 0 0
變化濃度:0.12 0.12 0.12 0.12
平衡時的濃度:0.08 0.18 0.12 0.12
則K=$\frac{0.12×0.12}{0.08×0.18}$=1,
故答案為:1;
(2)對于放熱反應,溫度越高,則化學平衡逆向移動,導致平衡常數減小,所以T1<300℃,即T1<573K,
故答案為:<;
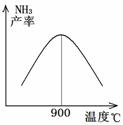
(3)對于放熱反應,溫度升高,則化學平衡向逆向移動,所以氨氣的產率減小,
故答案為:溫度高于900℃時,平衡向左移動;
(4)根據題意:①$\frac{1}{2}$CH4(g)+2NO2(g)═2NO(g)+$\frac{1}{2}$CO2(g)+H2O(g)△H=$\frac{1}{2}$×(-574kJ•mol-1)=-287kJ•mol-1;
$\frac{1}{2}$CH4(g)+2NO(g)═N2(g)+$\frac{1}{2}$CO2(g)+H2O(g)△H=$\frac{1}{2}$×(-1160kJ•mol-1)=-580kJ•mol-1;
根據蓋斯定律反應CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)可以看成是①+②,所以△H=-287kJ•mol-1-580kJ•mol-1=-867kJ•mol-1,
故答案為:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=-867kJ•mol-1;
(5)氨氣在純氧中燃燒,生成氮氣和水,在燃料電池中,燃料做負極,則通入氨氣的電極是負極,堿性條件下,該電極發生反應的電極反應式為2NH3-6e-+6OH-→N2+6H2O,
故答案為:2NH3-6e-+6OH-=N2+6H2O.
點評 本題是一道工業合成氨的綜合性知識題目,可以根據所學知識進行回答,難度較大.


科目:高中化學 來源: 題型:選擇題
| A. | 鐵溶于稀硝酸,溶液變黃:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| B. | Na2CO3溶液能使酚酞試液變紅:CO32-+H2O?HCO3-+OH- | |
| C. | 0.lmol•L-l CH3COOH溶液的pH>1:CH3COOH?CH3COO-+H+ | |
| D. | 向Mg(OH)2懸濁液中加入FeCl3溶液,出現紅褐色沉淀:3Mg(OH)2(s)+2Fe3+(aq)═2Fe( OH)3(s)+3Mg2+(aq) |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 相同 | |
| B. | 無法比較 | |
| C. | 依次為0.12mol/L、0.24mol/L、0.36mol/L | |
| D. | 依次為0.06mol/L、0.12mol/L、0.18mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | K+ Na+ NO3- CO32- | B. | Na十 Fe3+ SCN- SO42- | ||
| C. | K+ Na十 Cl- AlO2- | D. | Al3+ Na+ Cl- SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入水時,平衡向正反應方向移動,c(H+)增大 | |
| B. | 加入少量NaOH固體,平衡向正反應方向移動,c(H+)減少 | |
| C. | 加入少量0.1mol•L-1 HCl溶液,平衡向逆反應方向移動,溶液中c(H+)減少 | |
| D. | 加入少量CH3COONa固體,平衡向正反應方向移動,c(CH3COO-)增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 五種短周期元素的部分性質數據如下:
五種短周期元素的部分性質數據如下:| 元素 | T | X | Y | Z | W |
| 原子半徑(nm) | 0.037 | 0.075 | 0.099 | 0.102 | 0.143 |
| 最高或最低化合價 | +1 | +5,-3 | +7,-1 | +6,-2 | +3 |
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2g | B. | 4g | C. | 8g | D. | 10g |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com