
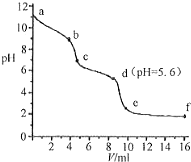
 常溫下,將已知濃度的鹽酸滴定到未知濃度的Na2CO3溶液,用pH傳感器測得混合溶液的pH變化曲線,如圖所示:(已知飽和CO2溶液的pH為5.6)下列說法正確的是( )
常溫下,將已知濃度的鹽酸滴定到未知濃度的Na2CO3溶液,用pH傳感器測得混合溶液的pH變化曲線,如圖所示:(已知飽和CO2溶液的pH為5.6)下列說法正確的是( )| A. | a點時,溶液呈堿性的原因是CO32-發生水解反應,其離子方程式為:CO32-+2H2O=H2CO3+2OH- | |
| B. | a→b段,溶液有氣體放出 | |
| C. | c點以后,鹽酸過量 | |
| D. | d點溶液中c(Na+)=c(Cl-) |
分析 A、碳酸根為弱酸根,水解分為兩步進行,且需要可逆號;
B、a→b段,碳酸鈉與鹽酸反應生成碳酸氫鈉,無二氧化碳氣體放出;
C、c點溶液的pH=7,此時溶液呈中性,據此解答即可;
D、d點為二氧化碳的飽和溶液,此時溶液中的溶質為NaCl,據此解答即可.
解答 解:A、碳酸根水解生成碳酸氫根,水解方程式為:CO32-+H2O?HCO3-+OH-,故A錯誤;
B、a→b段,碳酸鈉與鹽酸反應生成碳酸氫鈉,離子方程式為:CO32-+H+?HCO3-,無氣體放出,故B錯誤;
C、c點溶液的pH=7,此時溶液呈中性,鹽酸不過量,若鹽酸過量,溶液應呈酸性,故C錯誤;
D、d點為二氧化碳的飽和溶液,此時c(Na+)=c(Cl-),故D正確,故選D.
點評 本題主要考查的是酸與鹽的反應原理,涉及鹽類的水解、多元弱酸根與氫離子結合的原理、pH值的應用等,綜合性較強,有一定的難度.


 舉一反三單元同步過關卷系列答案
舉一反三單元同步過關卷系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河南省高一上月考二化學試卷(解析版) 題型:選擇題
下列關于物質分類的說法正確的是( )
A.SO2、CO、CO2都是酸性氧化物
B.BaSO4、Ca(OH)2、KNO3溶液都是電解質
C.純堿、燒堿、堿石灰都是堿
D.稀豆漿、牛奶、淀粉溶液都是膠體
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 反應過程中不可能產生H2 | |
| B. | 剩余的金屬粉末中一定有銅 | |
| C. | 往反應后的溶液中加入KSCN 溶液會變血紅色 | |
| D. | 往反應后的溶液中加入足量的稀H2SO4,則金屬粉末的質量一定會減少 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 若電解質 | H2CO3 | NH3•H2O |
| 電離平衡常數(25℃) | ${K}_{{a}_{1}}$=4.30×107 ${K}_{{a}_{2}}$=5.61×10-11 | Kh=1.77×10-5 |
| A. | 由數據可判斷該溶液呈酸性 | |
| B. | c(NH4+)>c(HCO32-)>c(CO32-)>c(NH3•H2O) | |
| C. | c(NH4+)+c(NH3•H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) | |
| D. | c(NH4+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 碳酸鈉的水解反應 CO32-+H2O→HCO3-+OH - | |
| B. | 碳酸氫鈣與過量的NaOH溶液反應Ca2++2HCO3-+2OH-→CaCO3↓+2H2O+CO32- | |
| C. | 苯酚鈉溶液與二氧化碳反應 C6H5O-+CO2+H2O→C6H5OH+CO32- | |
| D. | 稀硝酸與過量的鐵屑反應 3Fe+8H++2NO3-→3Fe3++2NO↑+4 H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.2molAl與足量NaOH溶液反應,生成的H2分子數為0.3NA | |
| B. | 常溫下,1LpH=1的鹽酸溶液,由水電離的H+離子數目為0.1NA | |
| C. | 鉛蓄電池中,當正極增加9.6g時,電路中通過的電子數目為0.2NA | |
| D. | 11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4 反應中,6 mol CuSO4能氧化白磷的分子數為1.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 ,
,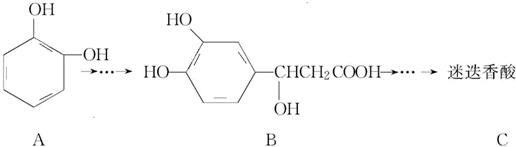
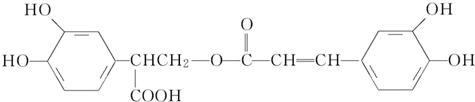
| A. | 有機物B可以發生取代、加成、消去、氧化反應 | |
| B. | 有機物A分子中所有原子一定在同一平面上 | |
| C. | 有機物C在濃硫酸催化下水解的一種產物是B | |
| D. | 1 mol B與足量的NaOH溶液反應,最多可消耗4 mol NaOH |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com