
分析 相等氧原子數,令O原子為1mol,則SO2為$\frac{1}{2}$mol,SO3為$\frac{1}{3}$mol;
(1)根據N=nNA計算;
(2)根據分子的物質的量結合分子組成計算;
(3)根據m=nM計算.
解答 解:相等氧原子數,令O原子為1mol,則SO2為$\frac{1}{2}$mol,SO3為$\frac{1}{3}$mol;
(1)由N=nNA可知,分子數目之比為$\frac{1}{2}$:$\frac{1}{3}$=3:2;
故答案為:3:2;
(2)SO2為$\frac{1}{2}$mol,SO3為$\frac{1}{3}$mol,則含有原子總數之比為($\frac{1}{2}$mol×3):($\frac{1}{3}$mol×4)=9:8;
故答案為:9:8;
(3)由m=nM可知,則分子質量之比為$\frac{1}{2}$×64:$\frac{1}{3}$×80=6:5,故答案為:6:5.
點評 本題考查物質的量的計算,側重于學生的計算能力的考查,有利于學習的積極性的培養,難度不大,注意相關計算公式的運用以及物質的分子構成.


科目:高中化學 來源: 題型:解答題

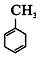 的官能團名稱為碳碳雙鍵.
的官能團名稱為碳碳雙鍵. 的系統命名為2-丙酮酸,則A的名稱是3-丁酮酸.
的系統命名為2-丙酮酸,則A的名稱是3-丁酮酸.
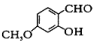 中能與稀NaOH溶液反應的官能團是羥基.檢驗該官能團的方法是取少量樣品,加入氯化鐵溶液,如果顯紫色,則說明含有酚羥基.
中能與稀NaOH溶液反應的官能團是羥基.檢驗該官能團的方法是取少量樣品,加入氯化鐵溶液,如果顯紫色,則說明含有酚羥基.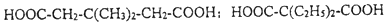 .
.
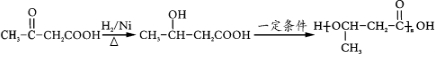 .(無機試劑任用)
.(無機試劑任用)查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②④ | B. | ②④⑤ | C. | ④⑥ | D. | ①③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
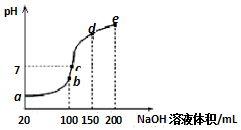 常溫下,現向50mL 0.1mol•L-1 NH4HSO4溶液中滴加0.05mol•L-1 NaOH溶液,得到溶液的pH與NaOH溶液體積的關系曲線如圖所示(假設滴加過程中無氣體產生).下列說法正確的是( )
常溫下,現向50mL 0.1mol•L-1 NH4HSO4溶液中滴加0.05mol•L-1 NaOH溶液,得到溶液的pH與NaOH溶液體積的關系曲線如圖所示(假設滴加過程中無氣體產生).下列說法正確的是( )| A. | b點溶液中離子濃度由大到小的順序為:c(Na+)>c(SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 圖中b、c、d、三點溶液中水的電離程度最大的是c點 | |
| C. | b點后滴加NaOH溶液過程中,NH3•H2O的電離程度逐漸減小 | |
| D. | pH=7時,溶液中c(H+)+c(Na+)+c(NH4+)=c(SO42-)+c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com