
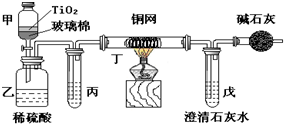
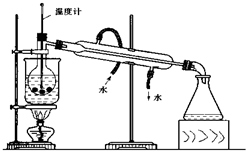
 未來生活中金屬鈦的運用越來越廣泛,如可在催化劑TiO2作用下,先用NaClO將CN-(毒性很強)氧化成CNO-,再在酸性條件下繼續被NaClO氧化成N2和CO2.環保工作人員在密閉系統中用如圖裝置進行實驗,以證明處理方法的有效性,并通過測定二氧化碳的量確定CN-被處理的百分率.將濃縮后含CN-離子的污水與過量NaClO溶液的混合液共200mL(其中CN-的濃度為0.05mol?L-1)倒入甲中,塞上橡皮塞,一段時間后,打開橡皮塞和活塞,使溶液全部放入乙中,關閉活塞.回答下列問題:
未來生活中金屬鈦的運用越來越廣泛,如可在催化劑TiO2作用下,先用NaClO將CN-(毒性很強)氧化成CNO-,再在酸性條件下繼續被NaClO氧化成N2和CO2.環保工作人員在密閉系統中用如圖裝置進行實驗,以證明處理方法的有效性,并通過測定二氧化碳的量確定CN-被處理的百分率.將濃縮后含CN-離子的污水與過量NaClO溶液的混合液共200mL(其中CN-的濃度為0.05mol?L-1)倒入甲中,塞上橡皮塞,一段時間后,打開橡皮塞和活塞,使溶液全部放入乙中,關閉活塞.回答下列問題:| 0.82g |
| 100g/mol |
| 0.0082mol |
| 0.01mol |


科目:高中化學 來源: 題型:
| A、2,3-二甲基-4-乙基己烷的名稱是正確的 |
| B、有機物CH3CO18OH和C2H5OH發生酯化反應的產物為CH3CO18OC2H5和H2O |
C、肌醇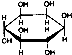 與葡萄糖 與葡萄糖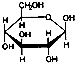 均含有六元環,互為同分異構體 均含有六元環,互為同分異構體 |
D、有機物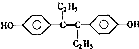 能發生加成反應,氧化反應和還原反應 能發生加成反應,氧化反應和還原反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
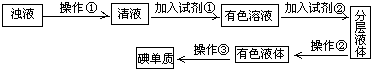
查看答案和解析>>
科目:高中化學 來源: 題型:
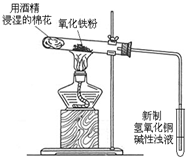 某課外小組同學做了如下探究實驗:將蘸有飽和氯化鐵溶液的粉筆,用坩堝鉗夾持置于酒精燈火焰上灼燒,一分鐘內可觀察到如下顏色變化:黃色(氯化鐵溶液)--紅褐色(A)--鐵銹紅色(B)--黑色(C).
某課外小組同學做了如下探究實驗:將蘸有飽和氯化鐵溶液的粉筆,用坩堝鉗夾持置于酒精燈火焰上灼燒,一分鐘內可觀察到如下顏色變化:黃色(氯化鐵溶液)--紅褐色(A)--鐵銹紅色(B)--黑色(C).查看答案和解析>>
科目:高中化學 來源: 題型:
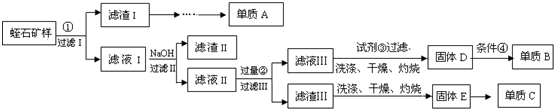
查看答案和解析>>
科目:高中化學 來源: 題型:
| C(H+) |
| C(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com