
 利用CH4和CO2可以制造價值更高的化學產品.已知下列反應:
利用CH4和CO2可以制造價值更高的化學產品.已知下列反應:分析 (1)利用已知熱化學方程式和待求熱化學方程式,據蓋斯定律解答;
(2)據反應物和生成物可知,參與大氣循環的無機化合物為二氧化碳,據原子守恒書寫化學方程式;
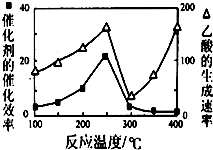
(3)①溫度超過250℃時,催化劑的催化效率降低,所以溫度升高而乙酸的生成速率降低;
②溫度升高,化學反應速率加快.
解答 解:(1)已知①CH4(g)+2O2(g)?CO2(g)+2H2O(g)△H1=a kJ/mol
②CO(g)+H2O(g)?CO2(g)+H2(g)△H2=b kJ/mol
③2CO(g)+O2(g)?2CO2(g)△H3=c kJ/mol
據蓋斯定律,①+2×②-2×③得:CH4(g)+CO2(g)?CO(g)+2H2(g)△H=(a+2b-2c)kJ/mol,
故答案為:a+2b-2c;
(2)據反應物和生成物可知,參與大氣循環的無機化合物為二氧化碳,據原子守恒書寫化學方程式為:3CO+3H2═CH3OCH3+CO2,
故答案為:3CO+3H2═CH3OCH3+CO2;
(3)①溫度超過250℃時,催化劑的催化效率降低,所以溫度升高而乙酸的生成速率降低,故答案為:催化劑的催化效率降低,化學反應速率降低;
②溫度升高,化學反應速率加快,故答案為:溫度升高,化學反應速率加快.
點評 本題考查了蓋斯定律的應用、氧化還原反應方程式書寫、影響反應速率的因素,綜合性但比較容易,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 互溶的液態混合物可用分液的方法分離 | |
| B. | 互不相溶的液態混合物可用分液的方法分離 | |
| C. | 沸點不同的液態混合物可用蒸餾的方法分離 | |
| D. | 氯化鈉和氧化銅形成的混合物可以按溶解、過濾、蒸發的順序分離 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 對于2SO2(g)+O2(g)?2SO3(g)△H=-QkJ/mol(Q>0),若向一密閉容器中加入1molSO2和0.5molO2充分反應后,放出的熱量為0.5QkJ | |
| B. | 熱化學方程式中的化學計量數表示相應物質的物質的量,不能用分數表示 | |
| C. | 需要加熱才能發生的反應不一定是吸熱反應 | |
| D. | 小蘇打在水中的電離方程式:NaHCO3═Na++H++CO${\;}_{3}^{2-}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 硅膠多孔,常用作食品干燥劑和催化劑的載體 | |
| B. | 用灼燒和聞氣味的方法區別棉織物和純毛織物 | |
| C. | 用SO2漂白過的草帽緶日久會變色 | |
| D. | 氯氣處理飲用水,在夏季的殺菌效果比在冬季好 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
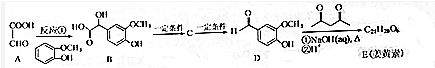
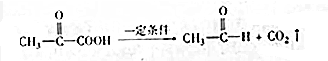


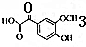
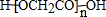
 ,
,查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 化學反應N2(g)+3H2(g)=2NH3(g)的能量變化如圖所示,請回答下列問題:
化學反應N2(g)+3H2(g)=2NH3(g)的能量變化如圖所示,請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋁制品的耐腐蝕性強,說明鋁的化學性質不活潑 | |
| B. | 化學反應速率的單位由時間單位和物質的量單位決定 | |
| C. | 離子鍵的本質是靜電作用,只能存在于由陰,陽離子構成的物質中 | |
| D. | 可將金屬鈉在研體中研成粉末,使鈉與水反應的實驗更安全 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 弱酸化學式 | CH3COOH | HCN | H2CO3 |
| 電離平衡常數(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
| A. | 等物質的量濃度的各溶液pH關系為:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) | |
| B. | a mol•L-1 HCN溶液與b mol•L-1 NaOH溶液等體積混合后,若所得溶液中c(Na+)>c(CN-),則a可能大于b | |
| C. | 冰醋酸中逐滴加水,則溶液的導電性、醋酸的電離度均先增大后減小 | |
| D. | NaHCO3溶液中,一定存在c(Na+)=c(HCO3-)+2c(CO32-)+c(H2CO3) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com