
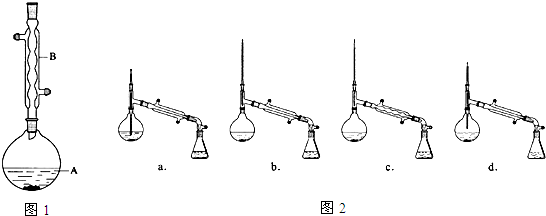
分析 (1)對于液體加熱蒸餾,應加入碎瓷片,防止暴沸;
(2)實驗室合成乙酸乙酯的實驗中濃硫酸作催化劑和吸水劑;
(3)乙酸、乙醇發生酯化反應生成乙酸乙酯;
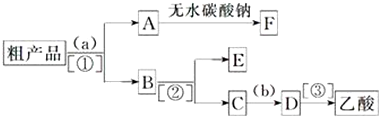
(4)粗產品乙酸乙酯中含有乙酸與乙醇,用飽和的碳酸鈉溶液反應掉乙酸,溶解乙醇,同時降低乙酸乙酯的溶解度,便于溶液分層,乙酸乙酯密度比水小,乙酸乙酯在上層,然后利用分液,乙酸乙酯加入無水碳酸鈉吸收其中的水,可得乙酸乙酯;溶液中含有乙醇、碳酸鈉、乙酸鈉,進行蒸餾可以收集乙醇,向蒸出乙醇的溶液中加入硫酸,可以得到乙酸,再進行蒸餾可以收集乙酸;
(5)得到的乙酸乙酯中加入無水碳酸鈉粉末,振蕩,除去乙酸乙酯的水份.
解答 解:(1)對于液體加熱蒸餾,應加入碎瓷片,防止暴沸;
故答案為:碎瓷片;防止暴沸;
(2)反應為可逆反應,加入濃硫酸,可起到催化劑的作用,且濃硫酸具有吸水性,有利于反應正向移動,故答案為:催化劑、吸水劑;
(3)乙酸、乙醇發生酯化反應生成乙酸乙酯,反應的化學方程式為CH3CH2OH+CH3COOH$→_{△}^{濃硫酸}$CH3CH2OOCCH3+H2O,
故答案為:CH3CH2OH+CH3COOH$→_{△}^{濃硫酸}$CH3CH2OOCCH3+H2O;
(4)粗產品乙酸乙酯中含有乙酸與乙醇,用飽和的碳酸鈉溶液反應掉乙酸,溶解乙醇,同時降低乙酸乙酯的溶解度,便于溶液分層,乙酸乙酯密度比水小,乙酸乙酯在上層,然后利用分液,乙酸乙酯加入無水碳酸鈉吸收其中的水,可得乙酸乙酯;溶液中含有乙醇、碳酸鈉、乙酸鈉,進行蒸餾可以收集乙醇,向蒸出乙醇的溶液中加入硫酸,可以得到乙酸,再進行蒸餾可以收集乙酸;
故答案為:飽和碳酸鈉溶液;稀硫酸;萃取分液;蒸餾;蒸餾;乙酸乙酯; 乙醇;
(5)分液得到的乙酸乙酯中含有水分,加入無水碳酸鈉粉末,振蕩,除去乙酸乙酯的水份.
故答案為:除去乙酸乙酯中的水.
點評 本題考查乙酸乙酯的制備,為高頻考點,側重于學生的分析能力和實驗能力的考查,難度不大,注意實驗混合液的配制、飽和碳酸鈉溶液的作用以及酯化反應的機理,(4)中試劑b選擇,由于鹽酸易揮發,不能使用鹽酸.


 學業測評一課一測系列答案
學業測評一課一測系列答案科目:高中化學 來源: 題型:選擇題
| A. | 少量的CO2通入NaClO溶液中發生反應:NaClO+CO2+H2O=NaHCO3+HClO,說明酸性強弱的順序為H2CO3>HClO>HCO3- | |
| B. | 金剛石是自然界中硬度最大的物質,不可能與氧氣發生反應 | |
| C. | 濃H2SO4具有強氧化性,常溫下就能與金屬Cu發生劇烈反應 | |
| D. | NO2與H2O 反應的過程中,被氧化的氮原子與被還原的氮原子的個數比為1:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
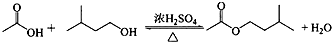
| 相對分子質量 | 密度/(g•cm-3) | 沸點/℃ | 水中溶解性 | |
| 異戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸異戊酯 | 130 | 0.8670 | 142 | 難溶 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| , | 實驗操作 | 預期現象 | 結 論 |
| 驗證猜想I] | 步驟①:取少量0.01mol/L 酸性KMnO4溶液,滴入所得溶液中 | 溶液紫紅色褪去 | 含有Fe2+ |
| 步驟②:另取少量所得溶液,滴加KI溶液和淀粉溶液 | 溶液不變為藍色 | 不含Fe3+ | |
| 驗證猜想Ⅱ | 將所得氣體通入如下裝置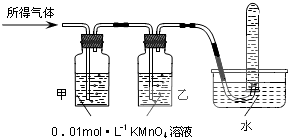 | 甲中KMnO4溶液褪色,乙中KMnO4溶液顏色不變,試管中收集到氣體 | 含有兩種氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
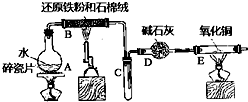 某實驗小組利用下圖所列裝置進行“鐵與水蒸氣反應”的實驗,并利用產物進一步制取FeCl3•6H2O晶體.(圖中夾持及尾氣處理裝置均已略去)請回答下列問題:
某實驗小組利用下圖所列裝置進行“鐵與水蒸氣反應”的實驗,并利用產物進一步制取FeCl3•6H2O晶體.(圖中夾持及尾氣處理裝置均已略去)請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
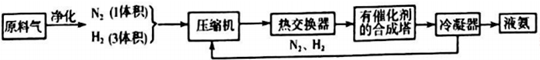
| 氣體 | CO | H2 | N2 | O2 |
| 體積(L) | 25 | 60 | 15 | 2.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com