
分析 根據常見的放熱反應有:所有的物質燃燒、金屬與酸或水反應、中和反應、鋁熱反應、絕大多數化合反應等;
常見的吸熱反應有:絕大數分解反應,以C、氫氣和CO為還原劑的氧化還原反應(如C和CO2),八水合氫氧化鋇與氯化銨的反應.
解答 解:①CaCO3分解是分解反應,故為吸熱反應,故正確;
②鈉與水反應是金屬和水的反應,故為放熱反應,故錯誤;
③所有的燃燒均為放熱反應,故硫在O2中燃燒放熱,故錯誤;
④CO2+C$\frac{\underline{\;\;△\;\;}}{\;}$2CO是吸熱反應,故正確;
⑤CaO+H2O═Ca(OH)2是化合反應,故為放熱反應,故錯誤;
⑥C+H2O(g)$\frac{\underline{\;高溫\;}}{\;}$CO+H2 是以碳為還原劑的氧化還原反應,故為吸熱反應,故正確;
⑦N2與H2合成NH3 是化合反應,故為放熱反應,故錯誤;
⑧NaOH和CH3COOH的反應是酸堿中和反應,故為放熱反應,故錯誤.
故答案為:①④⑥.
點評 本題考查吸熱反應和放熱反應,難度不大,明確常見的吸熱反應和放熱反應是解題的關鍵.


科目:高中化學 來源: 題型:選擇題
| A. | 若2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ•mol-1,則H2燃燒熱為241.8 kJ•mol-1 | |
| B. | 從C(石墨,s)═C(金剛石,s)△H=+1.9 kJ/mol,可知:金剛石比石墨更穩定 | |
| C. | 等質量的硫蒸氣和硫固體分別完全燃燒,后者放出熱量更多 | |
| D. | 化學反應中的能量變化,通常表現為熱量的變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②③④ | B. | ②④ | C. | ①③④ | D. | ①②④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 液氨中含有H2O,NH3•H2O,NH3,NH4+,NH2-等微粒 | |
| B. | 液氨中c(NH4+)•c(NH2-)是一個隨溫度升高而減小的常數 | |
| C. | 液氨的電離達到平衡時c(NH3)=c(NH4+)=c(NH2-) | |
| D. | 任何溫度下,只要不加入其他物質,液氨中c(NH4+)和c(NH2-)一定相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 任何濃度的溶液都可以用pH來表示其酸堿性的強弱 | |
| B. | 某溶液中由水電離出的c(OH-)=1×10-a mol•L-1,若a>7,則該溶液的pH一定為14-a | |
| C. | 0.2 mol•L-1 CH3COOH溶液中的c(H+)是0.1 mol•L-1 CH3COOH溶液中的c(H+)的2倍 | |
| D. | 無論是純水,還是酸性、堿性或中性稀溶液,在常溫下,其c(H+)•c(OH-)=1×10-14 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 由 1 mol CuFeS2 生成 1mol Cu,共消耗 2.75 molO2 | |
| B. | 該冶煉方法中產生大量的有害氣體SO2,可回收用于制備硫酸 | |
| C. | 在反應③中,Cu2S既是氧化劑,又是還原劑 | |
| D. | 在反應①中,SO2既是氧化產物,又是還原產物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
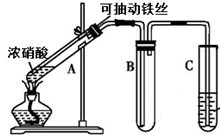 某校化學興趣小組利用如圖所示裝置進行探究鐵與濃硝酸的反應.
某校化學興趣小組利用如圖所示裝置進行探究鐵與濃硝酸的反應.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
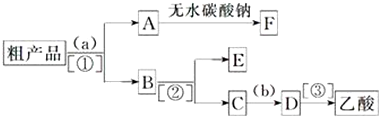
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
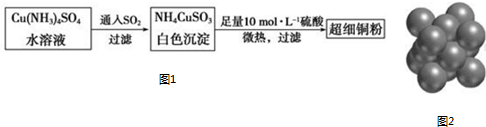
 ; NH4CuSO3中N、O、S三種元素的第一電離能由大到小順序為N>O>S(填元素符號).
; NH4CuSO3中N、O、S三種元素的第一電離能由大到小順序為N>O>S(填元素符號).查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com