
 (1)寫出制取乙酸乙酯的化學反應方程式CH3COOH+CH3CH2OH
(1)寫出制取乙酸乙酯的化學反應方程式CH3COOH+CH3CH2OH CH3COOC2H5+H2O;
CH3COOC2H5+H2O;分析 (1)酯化反應的本質為酸脫羥基,醇脫氫,在A中反應生成乙酸乙酯和水,且為可逆反應;
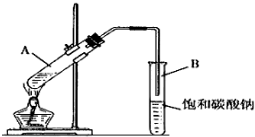
(2)從濃硫酸溶于水放熱和加熱時試管內液體的體積不超過試管容積的1/3”分析,加入藥品時,為防止酸液飛濺,應先加入乙醇再加入濃硫酸和乙酸;
(3)乙酸與乙醇需濃硫酸作催化劑,該反應為可逆反應,濃硫酸吸水利于平衡向生成乙酸乙酯方向移動;
(4)用飽和碳酸鈉溶液吸收乙酸乙酯,乙醇溶解,碳酸鈉與乙酸反應除去乙酸、同時降低乙酸乙酯的溶解度;
(5)根據粗產品乙酸乙酯、乙酸和乙醇的混合物中各自的性質,進行解答;
(6)根據化學平衡狀態的特征分析,當反應達到平衡狀態時,正逆反應速率相等,各物質的濃度、質量、體積分數以及百分含量不變,以及由此衍生的一些量也不發生變化.
解答 解:(1)酯化反應的本質為酸脫羥基,醇脫氫,在A中乙酸與乙醇在濃硫酸作用下加熱發生酯化反應生成乙酸乙酯和水,該反應方程式為:CH3COOH+CH3CH2OH CH3COOC2H5+H2O,
CH3COOC2H5+H2O,
故答案為:CH3COOH+CH3CH2OH CH3COOC2H5+H2O;
CH3COOC2H5+H2O;
(2)濃硫酸溶于水放出大量的熱,乙醇中含有少量水,應將濃硫酸加入到乙醇中,防止硫酸溶解時放出大量的熱導致液體飛濺,另外,加熱時,試管內液體的體積不超過試管容積的1/3”,加入藥品的順序為在一個30mL大試管中注入3mL乙醇,再分別緩緩加入2mL濃硫酸和3mL乙酸(乙酸和濃硫酸的加入順序可互換),邊加邊振蕩試管使之混合均勻(藥品總用量不能超過10mL),
故答案為:在一個30 mL的大試管中注入3 mL乙醇,再分別緩緩加入2 mL濃硫酸、3mL乙酸(乙醇和濃硫酸的加入順序不可互換),邊加邊振蕩試管使之混合均勻;
(3)乙酸與乙醇發生酯化反應,該反應為可逆反應,需濃硫酸作催化劑,濃硫酸吸水利于平衡向生成乙酸乙酯方向移動,故濃硫酸的作用為催化劑、吸水劑,
故答案為:催化作用、吸水作用;
(4)乙醇與乙酸都易揮發,制備的乙酸乙酯含有乙醇與乙酸,通常用飽和碳酸鈉溶液吸收乙酸乙酯,中和揮發出來的乙酸,使之轉化為乙酸鈉溶于水中,溶解揮發出來的乙醇,降低乙酸乙酯在水中的溶解度,便于分層得到酯;
故答案為:吸收除去揮發出來的乙酸和乙醇、降低乙酸乙酯的溶解度;
(5)乙酸乙酯中混有乙醇和乙酸,二者易溶于水而產生倒吸,導管不能插入到Na2CO3溶液中,防止倒吸回流現象的發生,
故答案為:防止倒吸;
(6)①單位時間內生成1mol乙酸乙酯,同時生成1mol水,都表示正反應速率,不能說明到達平衡狀態,故①錯誤;
②單位時間內生成1mol乙酸乙酯表示正反應,同時生成1mol乙酸表示逆反應,說明正逆反應速率相等,反應達到平衡狀態,故②正確;
③單位時間內消耗1mol乙醇,同時消耗1mol乙酸,都表示正反應速率,不能說明到達平衡狀態,故③錯誤;
④當反應達到平衡狀態時,正逆反應速率相等,故④正確;
⑤當反應達到平衡狀態時,混合物中各物質的濃度不再變化,故⑤正確.
故選②④⑤.
點評 本題考查乙酸乙酯的制備,題目難度不大,注意理解飽和碳酸鈉溶液的作用以及酯化反應的機理,試題培養了學生分析、理解能力及靈活應用所學知識解決實際問題的能力.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用系統命名:CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 | |
| B. | 2-甲基戊烷和2,2-二甲基丁烷互為同分異構體,C2H6和C3H8一定互為同系物 | |
| C. | 將(NH4)2SO4、CuSO4溶液分別加入蛋白質溶液,都出現沉淀,表明二者均可使蛋白質變性 | |
| D. | 糖類、油脂和蛋白質均可發生水解反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
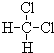 和
和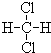 ;
;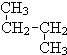 和
和 ⑦CH3 (CH2) 3CH3和
⑦CH3 (CH2) 3CH3和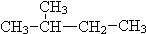
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 銅絲在乙醇中變黑 | B. | 銅絲點燃后變紅 | ||
| C. | 反應中產生黑煙 | D. | 銅絲在乙醇中變紅 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
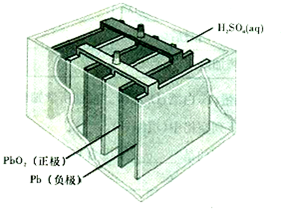
 如圖所示的直型石英玻璃封管中充有CO氣體,左端放置不純的鎳(Ni)粉.在一定條件下,Ni可以與CO(g)發生如下反應:Ni(s)+4CO(g)$?_{453~473K}^{323~353K}$Ni(CO)4(g)
如圖所示的直型石英玻璃封管中充有CO氣體,左端放置不純的鎳(Ni)粉.在一定條件下,Ni可以與CO(g)發生如下反應:Ni(s)+4CO(g)$?_{453~473K}^{323~353K}$Ni(CO)4(g)| A. | 在石英管右端主要物質是Ni(CO)4(g) | |
| B. | 在石英管右端主要物質是純Ni(s)和CO(g) | |
| C. | 在石英管左端主要物質是純Ni(s)和CO(g) | |
| D. | 整個過程可以看作CO(g)將Ni(s)從石英管左端轉移到右端,從而達到提純目的 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | A | B | C | D |
| n(CO2)(mol) | 1 | 1.5 | 2 | 3 |
| n(沉淀)(mol) | 0.5 | 1 | 1.5 | 1 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題


查看答案和解析>>
科目:高中化學 來源: 題型:解答題
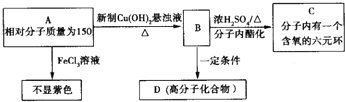
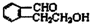 ;
;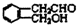 .
. ;此A對應的B生成C的反應:
;此A對應的B生成C的反應: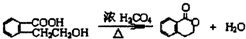 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com