
| A. | FeCl3溶液與Cu的反應:Cu+Fe3+═Cu2++Fe2+ | |
| B. | 向NaAlO2溶液中通入過量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| C. | 醋酸溶液與水垢中的CaCO3反應:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | NO2與水的反應:3NO2+H2O═2NO3-+NO+2H+ |
分析 A.電子、電荷不守恒;
B.反應生成氫氧化鋁和碳酸氫鈉;
C.醋酸在離子反應中保留化學式;
D.反應生成硝酸和NO.
解答 解:A.FeCl3溶液與Cu的反應的離子反應為Cu+2Fe3+═Cu2++2Fe2+,故A錯誤;
B.向NaAlO2溶液中通入過量CO2的離子反應為AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,故B錯誤;
C.醋酸溶液與水垢中的CaCO3反應的離子反應為CaCO3+2CH3COOH═2CH3COO-+Ca2++H2O+CO2↑,故C錯誤;
D.NO2與水的反應的離子反應為3NO2+H2O═2NO3-+NO+2H+,故D正確;
故選D.
點評 本題考查離子反應方程式書寫的正誤判斷,為高頻考點,把握發生的反應及離子反應的書寫方法為解答的關鍵,側重復分解反應、氧化還原反應的離子反應考查,注意離子反應中保留化學式的物質及電子、電荷守恒,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 實驗①和②均能證明K2Cr2O7溶液中存在上述平衡 | |
| B. | 實驗②能說明氧化性:Cr2O7 2->Fe3+ | |
| C. | 稀釋K2Cr2O7溶液時,溶液中各離子濃度均減小 | |
| D. | CrO42- 和Fe2+在酸性溶液中可以大量共存 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3Fe+4H2O(g)═Fe3O4+4H2 | B. | 2Na+2H2O═2NaOH+H2↑ | ||
| C. | 2F2+2H2O═4HF+O2? | D. | Cl2+2H2O═HClO+HCl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1L0.1mol/L的 Na2S溶液中S2-的個數為0.1NA | |
| B. | 標準狀況下,11.2LH2所含的中子數為0.15 NA | |
| C. | 7.8g Na2O2與足量的水反應,轉移的電子數為0.2 NA | |
| D. | 1mol羥基所含電子數為9 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 現象或事實 | 解釋或解決方法 |
| A | 大量的燃煤、燃油是形成霧霾的主要原因, | 發展核能等清潔能源,減少化石燃料的使用 |
| B | “地溝油”是被氧化、分解的油脂,禁止食用 | 采用化學技術處理后代替汽油作燃料 |
| C | 氫氧化鈉與氫氟酸都能與硅、二氧化硅反應 | 硅、二氧化硅都具有兩性 |
| D | 漂白粉在空氣中久置變質是 | 漂白粉中的有效成分與空氣中的CO2反應生成CaCO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
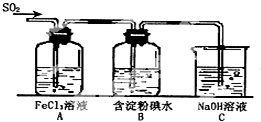 某興趣小組研究SO2氣體還原Fe3+、I2,他們使用的藥品和裝置如圖所示:
某興趣小組研究SO2氣體還原Fe3+、I2,他們使用的藥品和裝置如圖所示:查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 50mL 0.50mol/L H2SO4溶液與50mL 0.50mol/L Ba(OH)2溶液 | |
| B. | 50mL 0.50mol/L鹽酸溶液與50mL 0.50mol/L NaOH溶液 | |
| C. | 50mL 0.50mol/LCH3COOH溶液與50mL 0.50mol/L NaOH溶液 | |
| D. | 50mL 0.50mol/L鹽酸溶液與50mL 0.50mol/L氨水 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com