
| A. | pH=4的鹽酸與pH=10的氨水溶液等體積混合后pH>7 | |
| B. | 氯水中:c(Cl2)=2[c(ClO-)+c(Cl-)+c(HClO)] | |
| C. | pH=11的NaOH和pH=11的氨水分別稀釋100倍后的pH前者一定大于后者 | |
| D. | 0.10 mol•L-1 Na2CO3溶液:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
分析 A.氨水為弱堿,混合液中氨水過量,溶液呈堿性;
B.氯氣溶于水,只有部分氯氣與水反應,則氯水中仍然存在大量的氯氣分子;
C.氨水為弱堿,稀釋后期電離程度增大,則稀釋后氨水中氫氧根離子濃度大于氫氧化鈉;
D.根據碳酸鈉溶液中的電荷守恒判斷.
解答 解:A.pH=4的鹽酸與pH=10的氨水溶液等體積混合后,氨水為弱堿,則混合液中氨水過量,混合液呈堿性,溶液的pH>7,故A正確;
B.氯水中存在未參與反應的氯氣,則c(Cl2)≠2[c(ClO-)+c(Cl-)+c(HClO)],故B錯誤;
C.pH=11的NaOH和pH=11的氨水分別稀釋100倍,由于氨水的電離程度增大,則稀釋后氨水中氫氧根離子濃度較大,所以pH前者一定小于后者,故C錯誤;
D.0.10mol•L-1Na2CO3溶液中,根據電荷守恒可得:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),故D錯誤;
故選A.
點評 本題考查了離子濃度大小比較、溶液pH的計算,題目難度中等,明確弱電解質的電離平衡及其影響為解答關鍵,注意掌握電荷守恒的含義及應用方法,B為易錯點,注意氯水中還存在大量氯氣.


科目:高中化學 來源: 題型:選擇題
 2011國際化學年,為紀念瑞士化學家Reichstein 1933年首先合成維生素C,瑞士發行了一枚印有Vc分子(C6H8O6)的3D效果郵票(如右圖,圖中小短棍可表示單鍵、雙鍵或叁鍵).下列關于Vc說法正確的是( )
2011國際化學年,為紀念瑞士化學家Reichstein 1933年首先合成維生素C,瑞士發行了一枚印有Vc分子(C6H8O6)的3D效果郵票(如右圖,圖中小短棍可表示單鍵、雙鍵或叁鍵).下列關于Vc說法正確的是( )| A. | 維生素C結構中包含了一個五元碳環 | |
| B. | 從結構來看,維生素C不溶于水 | |
| C. | 維生素C具有羥基和酯基兩種官能團 | |
| D. | 維生素C能與氫氣、溴水、氫氧化鈉溶液等發生反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 同溫度,同體積的N2和O2 | B. | 同質量,不同密度的N2和CO | ||
| C. | 同壓強,同體積的H2和CH4? | D. | 同體積,同密度的CO2和N2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH4+、Mg2+、SO42-、CH3COO- | B. | HCO3-、K+、Cl-、AlO2- | ||
| C. | Cu2+、Na+、SO42-、HS- | D. | Na+、H+、SO42-、S2O32- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將滴有稀硫酸的淀粉溶液加熱后,加入新制的Cu(OH)2懸濁液,加熱,沒有紅色沉淀,說明淀粉在該條件下沒有水解 | |
| B. | 將銅與足量的濃硝酸反應生成的氣體干燥后收集,用冰水混合物冷卻降溫,研究溫度對化學平衡的影響 | |
| C. | 將混合氣體通過飽和Na2CO3溶液以便除去CO2中少量的SO2 | |
| D. | 某無色溶液中加入Ba(NO3)2溶液,再加稀鹽酸,沉淀不溶解,則原溶液中一定有SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2-甲基丁醛 CH3CH2 (CH3)CHCOH | B. | 硬酯酸甘油脂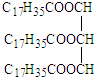 | ||
| C. | TNT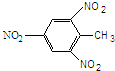 | D. | α-氨基丙酸 CH3CH(NH2)COOH |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該溶液顯中性 | |
| B. | 該溶液中:2 c(Al3+)+c(Fe2+)+c(H+ )=4 c(SO42-)+c(OH-) | |
| C. | 在空氣中蒸干并灼燒該溶液,最后所得的殘留固體為Al2O3、Fe2O3 | |
| D. | 向該溶液中加入Ba(OH)2溶液,當SO42-完全沉淀時,Al3+、Fe2+恰好被完全沉淀 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
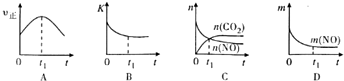
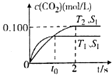 汽車尾氣凈化的主要原理為2NO(g)+2CO(g)$\stackrel{催化劑}{→}$2CO2+N2(g).在密閉容器中發生該反應時,c(CO2)隨溫度(T)、催化劑的表面積(S)和時間(t)的變化曲線如圖所示.據此判斷:
汽車尾氣凈化的主要原理為2NO(g)+2CO(g)$\stackrel{催化劑}{→}$2CO2+N2(g).在密閉容器中發生該反應時,c(CO2)隨溫度(T)、催化劑的表面積(S)和時間(t)的變化曲線如圖所示.據此判斷:| 容器編號 | 起始物質的量 | 平衡時物質的量 |
| Ⅰ | 2.0mol NO,2.0mol CO | 1.0mol CO2 |
| Ⅱ | 4.0mol NO,4.0mol CO |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com