
【題目】(1)鋅錳干電池是一種一次電池,外殼為金屬鋅,中間是碳棒,其周圍有碳粉,二氧化錳,氯化鋅和氯化銨等組成的填充物,該電池在放電過程產生MnOOH(難溶于水),回收處理該廢電池可以得到多種化工原料,有關數據下圖所示:
溶解度/(g/100g水)
溫度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-17 | 10-17 | 10-39 |
回答下列問題:
①普通鋅錳電池放電時發生的主要反應為:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH。該電池中,負極材料主要是________,正極發生的主要反應式是 。
加堿調節溶液pH,使溶液中氫氧根離子濃度達到 mol/L,鐵剛好完全沉淀(離子濃度小于1×10-5mol/L時,即可認為該離子沉淀完全)。繼續加堿調節pH為 ,鋅開始沉淀(假定Zn2+濃度為0.1mol/L)。
(2)在分析化學中常用Na2C2O4晶體(溶液無色)作為基準物質測定KMnO4溶液的濃度。在H2SO4溶液中,反應如下:2MnO+5C2O+16H+![]() 2Mn2+(溶液無色)+10CO2↑+8H2O。
2Mn2+(溶液無色)+10CO2↑+8H2O。
①若將W g Na2C2O4配成100 mL標準溶液,移取20.00 mL置于錐形瓶中,則酸性KMnO4溶液應裝在__________(填“酸式”或“堿式”)滴定管中。本次滴定 選擇指示劑(填“需要”、“不需要”)。判斷滴定達終點的現象是____ ___。
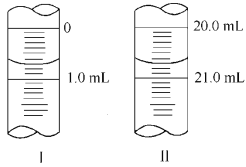
②若滴定管起始讀數和終點讀數如圖所示,則酸性KMnO4的物質的量濃度為_ (填表達式)。
③若滴定完畢立即讀數,測定的KMnO4溶液的濃度___(填“偏高”、“偏低”或“不變”)。
![]() 【答案】(1)①Zn;MnO2+e-+NH4+=MnOOH+NH3↑ ②5×10-12;6 ①酸式;不需要 滴入一滴酸性KMnO4溶液,溶液由無色變為紫色,且半分鐘內不褪色 ②
【答案】(1)①Zn;MnO2+e-+NH4+=MnOOH+NH3↑ ②5×10-12;6 ①酸式;不需要 滴入一滴酸性KMnO4溶液,溶液由無色變為紫色,且半分鐘內不褪色 ②![]() mol/L ③偏低
mol/L ③偏低
【解析】
試題分析:(1)①酸性鋅錳干電池是一種一次電池,外殼為金屬鋅,鋅是活潑的金屬,鋅是負極。中間是碳棒,碳棒是正極,其中二氧化錳得到電子轉化為MnOOH,根據總反應式可知正極電極反應式為MnO2+e-+NH4+=MnOOH+NH3↑。
②雙氧水具有強氧化性,能把鐵氧化為鐵離子,因此加入稀硫酸和雙氧水,溶解后鐵變為硫酸鐵。根據氫氧化鐵的溶度積常數可知,當鐵離子完全沉淀時溶液中鐵離子濃度為10—5mol/L,則溶液中氫氧根的濃度=![]() 。Zn2+濃度為0.1mol/L,根據氫氧化鋅的溶度積常數可知開始沉淀時的氫氧根濃度為=
。Zn2+濃度為0.1mol/L,根據氫氧化鋅的溶度積常數可知開始沉淀時的氫氧根濃度為=![]() =10—8mol/L,氫離子濃度是10—6mol/L,pH=6,即繼續加堿調節pH為6時鋅開始沉淀。
=10—8mol/L,氫離子濃度是10—6mol/L,pH=6,即繼續加堿調節pH為6時鋅開始沉淀。
(2)①由于KMnO4具有強氧化性,可腐蝕乳膠管,故KMnO4應裝入酸式滴定管中。由于酸性高錳酸鉀顯紫色,因此不需要指示劑。當達到終點時,再滴入一滴KMnO4溶液,溶液由無色變為紫色,且半分鐘內不褪色,說明反應達到滴定終點。
②由示意圖可知V(KMnO4)=20.70 mL-0.70 mL=20.00 mL,設KMnO4的物質的量濃度為x,則:
2MnO4- ~ ~ ~ 5C2O42-
2 5
20.00×10-3 L·x ![]()
解答x=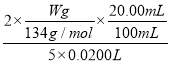 =
=![]() mol/L。
mol/L。
③溶液變色因局部過量而實際未達終點,立即讀數會造成V(KMnO4)減小,所以結果偏低。


科目:高中化學 來源: 題型:
【題目】實驗室制取乙烯并檢驗乙烯性質的裝置如下圖。

請回答有關問題:
(1)燒瓶中除反應物以外,還應放2-3塊碎瓷片,目的是_________________;
(2)燒瓶中產生乙烯的反應方程式為:_________________,反應類型為:_________________;C中發生反應的化學方程式為:_________________,反應類型為:_________________;
(3)反應一段時間后,可觀察到D中的現象是:_________________;
(4)B中所裝的溶液是:_________________溶液,起的作用是_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗題:綠礬(FeSO4·7H2O)是治療缺鐵性貧血藥品的重要成分。下列是以市售鐵屑(含少量錫、氧化鐵等雜質)為原料生產純凈綠礬的一種方法。

已知:室溫下飽和 H2S溶液的 pH 約為3.9,SnS沉淀完全時溶液的 pH 為1.6;FeS開始沉淀時溶液的 pH 為3.0,沉淀完全時的 pH 為5.5。
(1) 操作Ⅱ,在溶液中用硫酸酸化至 pH=2的目的是_______________________。
(2)操作Ⅳ的順序依次為________、________、過濾、洗滌、干燥。
(3)操作Ⅳ得到的綠礬晶體用少量冰水洗滌,其目的是:
①除去晶體表面附著的硫酸等雜質;
②________________________________________________________________________。
(4)測定綠礬產品中Fe2+含量的方法是
a.稱取一定質量的綠礬產品,配制成250.00 mL溶液;
b.量取25.00 mL 待測溶液于錐形瓶中;
c.用硫酸酸化的 0.010 00 mol·L-1 KMnO4溶液滴定至終點,消耗KMnO4溶液體積的平均值為20.00 mL。
滴定時發生反應的離子方程式為5Fe2++MnO4-+8H+===5Fe3++Mn2++4H2O
①用硫酸酸化的 0.010 00 mol·L-1 KMnO4溶液滴定時,左手把握酸式滴定管的活塞,右手搖動錐形瓶,眼睛注視錐形瓶中溶液顏色的變化判斷此滴定實驗達到終點的方法是___________________;
②若用上述方法測定的樣品中FeSO4·7H2O的質量分數偏低(測定過程中產生的誤差可忽略),其可能原因有___ _。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲醇是重要的化工原料,又可稱為燃料。利用合成氣(主要成分為CO、CO2和H2)在催化劑的作用下合成甲醇,發生的主反應如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H1〈0
CH3OH(g) △H1〈0
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g)![]() CO(g)+H2O(g) △H3〉0
CO(g)+H2O(g) △H3〉0
回答下列問題:
(1)反應①的化學平衡常數K的表達式為 ;圖1中能正確反映平衡常數K隨溫度變化關系的曲線為 (填曲線標記字母),其判斷理由是 。

(2)合成氣的組成n(H2)/n(CO+CO2)=2.60時體系中的CO平衡轉化率(a)與溫度和壓強的關系如圖2所示。a(CO)值隨溫度升高而 (填“增大”或“減小”),其原因是 。圖2中的壓強由大到小為_____,其判斷理由是_____。
(3)Bodensteins研究了下列反應:2HI(g)![]() H2(g)+I2(g)
H2(g)+I2(g)
在716K時,氣體混合物中碘化氫的物質的量分數x(HI)與反應時間t的關系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0. 784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
上述反應中,正反應速率為v正= k正·x2(HI),逆反應速率為v逆=k逆·x(H2)·x(I2),其中k正、k逆為速率常數, 其中k正、k逆為速率常數,則k逆為________(以K和k正表示)。若k正 = 0.0027min-1,在t=40min時,v正=__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面兩套實驗裝置,都涉及金屬的腐蝕反應,假設其中的金屬塊和金屬絲都是足量的。請同學們仔細觀察,完成18~19題。

(1)下列敘述正確的是
A.裝置Ⅰ在反應過程中自始至終只生成紅棕色氣體
B.裝置Ⅱ開始階段鐵絲只發生析氫腐蝕
C.裝置Ⅱ在反應過程中能產生氫氣
D.裝置Ⅰ在反應結束時溶液中的金屬陽離子只有Cu2+
(2)下列與反應原理相關的敘述不正確的是
A.裝置Ⅰ中不可能發生如下反應:Fe+2Fe3+= 3Fe2+
B.裝置Ⅱ在反應結束時溶液中存在Fe2+
C.裝置Ⅰ的溶液若換為稀硝酸,則腐蝕過程與原裝置不同
D.裝置Ⅱ中的鐵絲能發生電化學腐蝕
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(15分)按要求回答下列有關問題。
(1)據報道,科學家新研發出一種常溫下催化合成NH3的方法:2N2(g)+6H2O(l)=4NH3(g)+3O2(g)
已知如下信息:
①化合物的生成熱可以表示其相對能量。化學上,規定標準狀況下穩定單質的生成熱為0。幾種物質的生成熱:NH3(g)為mkJ·mol-1,H2O(l)為nkJ·mol-1。
反應的△H=產物的生成熱之和---反應物的生成熱之和
②幾種化學鍵的鍵能數據如下:
![]()
上述反應中,△H=_______kJ·mol-1,H-N鍵的鍵能為_______kJ·mol-1。
(2)二氧化硫在一定條件下可以發生如下反應:
SO2(g)+NO2(g)![]() SO3(g)+NO(g),△H= -42kJ·mol-1,在1L恒容密閉容器中充入SO2(g)和NO2(g),所得實驗數據如下:
SO3(g)+NO(g),△H= -42kJ·mol-1,在1L恒容密閉容器中充入SO2(g)和NO2(g),所得實驗數據如下:
實驗編號 | 溫度 | 起始時物質的量/mol | 平衡時物質的量/mol | |
N(SO2) | N(NO2) | N(NO) | ||
甲 | T1 | 0.80 | 0.20 | 0.18 |
乙 | T2 | 0.20 | 0.80 | 0.16 |
丙 | T3 | 0.20 | 0.30 | a |
①實驗甲中,若2min時測得放出的熱量是4.2kJ,則0~2min時間內,用SO2(g)表示的平均反應速率v(SO2)=_____________________;
②實驗丙中,達到平衡時,NO2的轉化率為____________;
③由表中數據可推知,Tl______T2(填“>”“<’’或“=”);
(3)對反應N2O4(g)![]() 2NO2(g) △H>0 在溫度為Tl、T2時平衡體系中NO2的體積分數隨壓強變化曲線如圖所示,下列說法正確的是__________。
2NO2(g) △H>0 在溫度為Tl、T2時平衡體系中NO2的體積分數隨壓強變化曲線如圖所示,下列說法正確的是__________。

a.A、C兩點的反應速率:A>C
b.A、C兩點氣體的顏色:A深,C淺
c.由狀態A到狀態B,可以用加熱的方法
d.A、C兩點的化學平衡常數:A=C
(4)工業上,采用石墨、鐵棒作為電極,電解除去廢水中的CN-(N為-3價,下同)

①鐵電極應連接直流電源的____________(填寫電極名稱)。
②上述反應方程式配平后“□”內應填寫________;
③陽極上發生的電極反應為2Cl--2e-=Cl2↑和_______________;
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA表示阿伏加德羅常數的值。下列說法中正確的有兒項( )
①1L0.1mol/LK2Cr2O7溶液中Cr2O72-的數目小于0.1NA
②1molCl2做氧化劑時得到的電子數為2NA
③25℃時,1LpH=12的碳酸鈉溶液中含有Na+的數目為0.02NA
④過氧化鈉與水反應時,生成0.5molO2轉移的電子數為2NA
⑤50mL18.4mol/L的濃硫酸與足量的銅微熱后反應,生成SO2分子數小于0.46NA
⑥利用氰尿酸與次氯酸在一定pH下反應可制備三氯異氰尿酸(結構如圖).若原料完全反應,得到1mol產物同時生成3NA個H2O

A.2 C.4 B.3 D.5
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ、 下列各組物質:①O2和O3 ②H2、D2、T2 ③12 C和14 C ④CH3CH2CH2CH3和(CH3)2CHCH3 ⑤癸烷和十六烷 ⑥CH3(CH2)5CH3和CH3CH2CH2CH(CH3)C2H5 (在橫線上填相應的序號)

A、互為同位素的是_________ ; B、互為同分異構體的是________;
C、互為同素異形體的是________; D、同一種物質的是_________。
Ⅱ、 寫出下列烷烴的分子式
(1)含有30個氫原子的烷 ;
(2)假如某烷烴的相對分子質量為142,則該烷烴的分子式為 ;
(3)烷烴A在同溫同壓下蒸氣的密度是H2的36倍 ;
(4)1L烷烴D的蒸氣完全燃燒時,生成同溫同壓下15L水蒸氣 。
Ⅲ、甲烷的電子式為________,碳氫鍵之間鍵角為 。甲烷和氯氣在光照下發生取代反應,生成___________種產物。產物中_________常用作滅火劑。試寫出三溴甲烷在光照條件下與溴蒸氣反應的化學方程式:____________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有七種元素,其中A、B、C、D、E為短周期主族元素,F、G為第四周期元素,它們的原子序數依次增大。請根據下列相關信息,回答問題。

(1)寫出BA3的電子式___________;
(2)B元素基態原子中能量最高的電子,其電子云在空間有________個取向,原子軌道呈_____形;
(3)某同學根據上述信息,推斷C基態原子的核外電子排布圖為![]() ,該同學所畫的電子排布圖違背了___________;
,該同學所畫的電子排布圖違背了___________;
(4)G位于_____族______區,該元素的核外電子排布式為___________;
(5)DE3中心原子的雜化方式為________,用價層電子對互斥理論推測其空間構型為___________;
(6)檢驗F元素的方法是___________,請用原子結構的知識解釋產生此現象的原因___________;
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com