

分析 (1)反應中只有I元素化合價發生變化,分別由+5價、-1價變化為0價,根據化合價變化確定電子轉移情況;
(2)反應②中C元素化合價由+3價升高到+4價,被氧化,H2C2O4為還原劑,Mn元素化合價由+7價降低到+2價,為氧化劑,結合化合價的變化解答.
解答 解:(1)氧化還原反應KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O中,電子轉移情況如下: ,故答案為:
,故答案為: ;
;
(2)反應②中C元素化合價由+3價升高到+4價,被氧化,H2C2O4為還原劑,Mn元素化合價由+7價降低到+2價,為氧化劑,
n(CO2)=$\frac{44.8×1{0}^{-3}L}{22.4L/mol}$=0.002mol,由方程式可知消耗氧化劑n(KMnO4)=0.002mol×$\frac{2}{10}$=0.0004mol,轉移電子的物質的量為0.0004mol×(7-2)=0.005mol,
n(CaC2O4)=n(H2C2O4)=$\frac{1}{2}$n(CO2)=0.001mol,
n(Ca)=n(CaC2O4)=0.001mol,
m(Ca)=0.001mol×40g/mol=0.04g,
故答案為:H2C2O4;0.0004mol;0.005mol;0.04.
點評 本題考查氧化還原反應計算,側重于學生的分析能力和計算能力的考查,為高考常見題型,把握反應中元素的化合價變化為解答的關鍵,題目難度不大.


 每課必練系列答案
每課必練系列答案 巧學巧練系列答案
巧學巧練系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
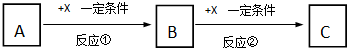
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
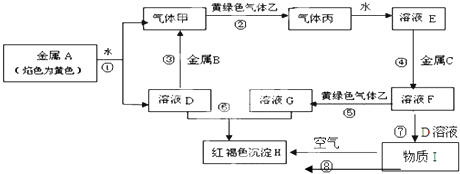
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2NO+O2═2NO2 | B. | 3NO2+H2O═2HNO3+NO | ||
| C. | 3H2+N2$?_{催化劑}^{高溫高壓}$3NH3 | D. | NH3+HNO3═NH4NO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
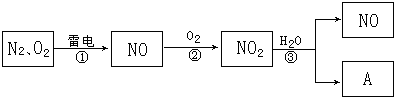
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
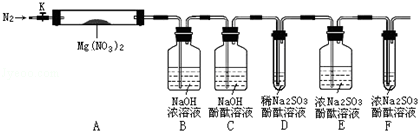
 ,步驟Ⅱ中,通入一段時間N2的目的是避免對分解產物O2的檢驗產生干擾.
,步驟Ⅱ中,通入一段時間N2的目的是避免對分解產物O2的檢驗產生干擾.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
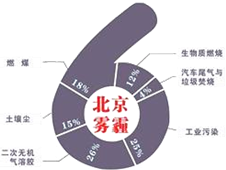 中科院大氣研究所研究員張仁健課題組與同行合作,對北京地區PM2.5有6個重要來源,其中,汽車尾氣和燃煤分別占4%、18%.用于凈化汽車尾氣的反應為2NO(g)+2CO(g)$\stackrel{催化劑}{?}$ 2CO2(g)+N2(g),已知該反應在570K時平衡常數為1×1059,但反應很慢.下列說法正確的是( )
中科院大氣研究所研究員張仁健課題組與同行合作,對北京地區PM2.5有6個重要來源,其中,汽車尾氣和燃煤分別占4%、18%.用于凈化汽車尾氣的反應為2NO(g)+2CO(g)$\stackrel{催化劑}{?}$ 2CO2(g)+N2(g),已知該反應在570K時平衡常數為1×1059,但反應很慢.下列說法正確的是( )| A. | 裝有尾氣凈化裝置的汽車排出的氣體中不再含有NO或CO | |
| B. | 提高尾氣凈化效率的常用方法是升高溫度 | |
| C. | 增大壓強,上述平衡右移,故實際操作中可通過增壓的方式提高其凈化效率 | |
| D. | 提高尾氣凈化效率的最佳途徑是使用高效催化劑 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com