
分析 (1)①根據配制一定物質的量濃度的溶液的操作步驟判斷:在配制物質的量濃度的溶液時,要經過:計算→稱量→溶解→移液、洗滌→振蕩→定容→搖勻等步驟;
A.沒有洗滌燒杯和玻璃棒,導致配制的溶液中溶質的物質的量偏小;
B.選用的容量瓶內有少量蒸餾水,不影響沉淀結果;
C.如果加水超過了刻度線,吸出水使液面恰好到刻度線,導致容量瓶中溶質的物質的量偏小,濃度偏低;
D.整個配制過程中,容量瓶不振蕩,會導致配制的溶液體積偏小,溶液濃度偏高;
②鋅粉能與Fe3+反應,加入鋅粉的目的是將Fe3+恰好還原成Fe2+;
③根據物質的性質和書寫離子方程式的有關要求書寫離子方程式;
④根據離子方程式計算,n(Fe)=5n(MnO4-)=5×$\frac{20.02mL+19.98mL}{2}$×0.01mol•L-1×10-3×10=1.0×10-2mol,m(Fe)=56 g•mol-1×1.0×10-2mol=0.56g.晶體中鐵的質量分數=$\frac{0.56g}{5g}$×100%=11.2%,若在步驟二中滴入酸性高錳酸鉀溶液不足,則會有部分草酸根離子未被氧化,在步驟三中則會造成消耗酸性高錳酸鉀溶液的量偏大,從而計算出的鐵的量增多,含量偏高;
(2)加熱后的晶體要在干燥器中冷卻,防止重新吸收空氣中的水分.另外在加熱時至少要稱量兩次質量差,到兩次稱量質量差不超過0.1 g.
解答 解:(1)①在配制物質的量濃度的溶液時,要經過:計算→稱量→溶解→移液、洗滌→振蕩→定容→搖勻等步驟;
A.沒有洗滌燒杯和玻璃棒,則配制的溶液中溶質的物質的量偏小,配制的溶液濃度偏低,故A正確;
B.選用的容量瓶內有少量蒸餾水,對溶質和最終配制溶液體積不影響,則不影響沉淀結果,故B錯誤;
C.如果加水超過了刻度線,吸出水使液面恰好到刻度線,導致容量瓶中溶質的物質的量偏小,配制的濃度偏低,故C正確;
D.整個配制過程中,容量瓶不振蕩,先加入的是密度較大的溶液,后加入的洗滌燒杯和玻璃棒的溶液密度較小,造成溶液密度不均勻,如果搖均勻密度大的和密度小的相溶體積會比二者原體積之和小,配制的溶液濃度偏高,故D錯誤;
故答案為:溶解;定容;AC;
②加入鋅粉的目的是將Fe3+恰好還原成Fe2+,
故答案為:將Fe3+恰好還原成Fe2+;
③在步驟三中發生的離子反應為:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,
故答案為:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
④根據步驟三中的離子反應可知:n(Fe)=5n(MnO4-)=5×$\frac{20.02mL+19.98mL}{2}$×0.01 mol•L-1×10-3×10=1.0×10-2mol,m(Fe)=56 g•mol-1×1.0×10-2mol=0.56g.晶體中鐵的質量分數為:$\frac{0.56g}{5g}$×100%=11.20%,
若在步驟二中滴入酸性高錳酸鉀溶液不足,則會有部分草酸根離子未被氧化,在步驟三中則會造成消耗酸性高錳酸鉀溶液的量偏大,從而計算出的鐵的量增多,含量偏高,
故答案為:11.20%或0.112;偏高;
(2)加熱后的晶體要在干燥器中冷卻,防止重新吸收空氣中的水分.另外在加熱時至少要稱量兩次質量差,到兩次稱量質量差不超過0.1 g,故答案為:加熱后的晶體要在干燥器中冷卻; 兩次稱量質量差不超過0.1 g.
點評 本題考查探究物質組成、測量物質含量的方法,題目難度中等,涉及到溶液的配制、滴定和結晶等操作、質量分數的計算等知識,注意基礎實驗知識的積累,把握實驗步驟、原理和注意事項等問題.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 晶格能大小:NaI>NaBr>NaCl>NaF | B. | 單質的熔點:Li<Na<K<Rb | ||
| C. | 共價鍵的鍵能:C-C>C-Si>Si-Si | D. | 沸點高低:HF<HCl<HBr<HI |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C的燃燒熱為Q1 kJ/mol | |
| B. | 2 mol CO(g)所具有的能量一定高于2 mol CO2(g)所具有的能量 | |
| C. | 一定質量的C燃燒,生成CO2(g)比生成CO(g)時放出的熱量多 | |
| D. | C燃燒生成CO2氣體的熱化學方程式為:C(s)+O2(g)═CO2(g)△H=-(Q1+Q2) kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
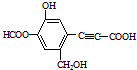
| A. | 該有機物分子式為:C11H10O6 | |
| B. | 分子中最多有9個碳原子共平面 | |
| C. | 該有機物可發生取代反應、還原反應,不能發生銀鏡反應 | |
| D. | 1 mol該有機物分別與足量Na、NaOH溶液、NaHCO3溶液完全反應,消耗Na、NaOH、NaHCO3的物質的量分別為3mol、4mol、1 mol |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
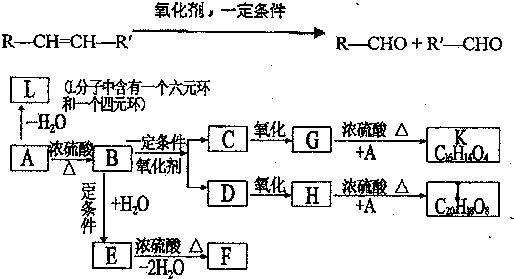
 、K
、K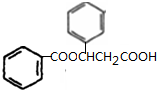 ;
; $→_{△}^{濃硫酸}$
$→_{△}^{濃硫酸}$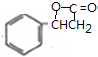 +H2O,反應類型取代反應或酯化反應;
+H2O,反應類型取代反應或酯化反應;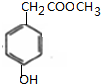 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
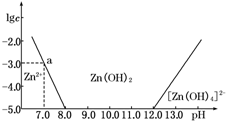 如圖所示,橫坐標為溶液的pH,縱坐標為Zn2+或[Zn(OH)4]2-的物質的量濃度的對數.回答下列問題:
如圖所示,橫坐標為溶液的pH,縱坐標為Zn2+或[Zn(OH)4]2-的物質的量濃度的對數.回答下列問題:| c(HCl) | |||||||
| (mol/L) | 0.50 | 1.00 | 2.04 | 2.90 | 4.02 | 5.16 | 5.78 |
| 103 c(PbCl2) | |||||||
| (mol/L) | 5.10 | 4.91 | 5.21 | 5.90 | 7.48 | 10.81 | 14.01 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
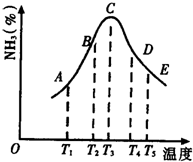 (1)在容積不同的密閉容器內,分別充入同量的N2和H2,在不同溫度下,任其發生反應N2+3H2?2NH3,并分別在t秒時測定其中NH3的體積分數,繪圖如圖:
(1)在容積不同的密閉容器內,分別充入同量的N2和H2,在不同溫度下,任其發生反應N2+3H2?2NH3,并分別在t秒時測定其中NH3的體積分數,繪圖如圖:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 $→_{△}^{KMnO_{4}/H+}$
$→_{△}^{KMnO_{4}/H+}$
 $\stackrel{一定條件下}{→}$
$\stackrel{一定條件下}{→}$ (苯胺,弱堿性,易被氧化)化合物C是制取消炎靈(祛炎痛)的中間產物,其合成路線如圖所示:
(苯胺,弱堿性,易被氧化)化合物C是制取消炎靈(祛炎痛)的中間產物,其合成路線如圖所示:
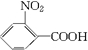 .
. ;
; .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com