
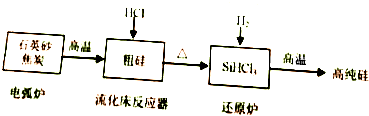
 硅在地殼中的含量較高.硅及其化合物的開發由來已久,在現代生活中有廣泛應用,回答下列問題:
硅在地殼中的含量較高.硅及其化合物的開發由來已久,在現代生活中有廣泛應用,回答下列問題:| 物質 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸點/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
| ||
| ||
| ||
| ||
| ||
| ||


 小學課堂作業系列答案
小學課堂作業系列答案 金博士一點全通系列答案
金博士一點全通系列答案科目:高中化學 來源: 題型:
| A、Y、Z、X、W的原子序數依次減小 |
| B、W與X可形成既含極性共價鍵又含非極性共價鍵的化合物 |
| C、由W、X、Y、Z四種元素組成的常見化合物一定顯酸性 |
| D、X的簡單氫化物的沸點低于Y的簡單氫化物的沸點 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 X、Y、Z、W都是中學化學常見的物質,其中X、Y、Z均含有同一種元素.在一定條件下相互轉化的關系如圖所示(部分反應中的H2O已略去).請按要求回答下列問題:
X、Y、Z、W都是中學化學常見的物質,其中X、Y、Z均含有同一種元素.在一定條件下相互轉化的關系如圖所示(部分反應中的H2O已略去).請按要求回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:
| 離子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 濃度(mol/L) | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |

| ||
| 放電 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 合成氨對農業生產及國防建設均具有重要意義.
合成氨對農業生產及國防建設均具有重要意義.查看答案和解析>>
科目:高中化學 來源: 題型:
| 結構簡式 | 化學式 | 相對分子質量 | 沸點/℃ |
| (1)H-OH | H2O | 18 | 100 |
| (2)CH3-OH | CH4O | 32 | 64 |
| (3)CH3CH2OH | C2H6O | 46 | 78 |
| (4)CH3COOH | C2H4O2 | 60 | 118 |
| (5)CH3-O-CH3 | C2H6O | 58 | 56 |
| (6)CH3CH2CH2OH | C3H8O | 60 | 97 |
| (7)CH3CH2OCH3 | C3H8O | 60 | 11 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 某課外活動小組利用下列裝置迅速制備少量氯氣.提供的試劑有:濃鹽酸、飽和食鹽水、氫氧化鈉溶液、高錳酸鉀固體.(2KMnO4+16HCl(濃)═2KCl+2MnCl2+5Cl2↑+8H2O)試回答:
某課外活動小組利用下列裝置迅速制備少量氯氣.提供的試劑有:濃鹽酸、飽和食鹽水、氫氧化鈉溶液、高錳酸鉀固體.(2KMnO4+16HCl(濃)═2KCl+2MnCl2+5Cl2↑+8H2O)試回答:查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、在盛有苯的試管中加入幾滴酸性KMnO4溶液,可觀察到紫色褪去 |
| B、向雞蛋清溶液中滴加飽和CuSO4溶液,有固體析出,再加入足量蒸餾水,固體可以重新溶解 |
| C、用燈光照射盛有CH4與Cl2(體積比1:4)的集氣瓶后,可觀察到瓶內壁附有液態物質 |
| D、將紅熱的銅絲迅速插入乙醇中,可觀察到銅絲表面變黑,反復多次,并能聞到香味 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com