
| 0.7493225g |
| 0.7500g |


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
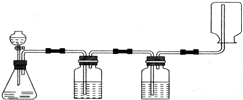 某學生在實驗室做氣體發生、洗滌、干燥、收集(不考慮尾氣的處理)實驗,裝置圖如圖示.該同學所做的實驗是( )
某學生在實驗室做氣體發生、洗滌、干燥、收集(不考慮尾氣的處理)實驗,裝置圖如圖示.該同學所做的實驗是( )| A、鋅和鹽酸反應制取氫氣 |
| B、二氧化錳和濃鹽酸反應制取氯氣 |
| C、碳酸鈣和鹽酸反應制取二氧化碳 |
| D、過氧化鈉和水反應制取氧氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| 名稱 | 托盤天平(帶砝碼) | 小燒杯 | 坩堝鉗 | 玻璃棒 | 鑰匙 | 量筒 |
| 儀器 |  |  |  |  |  |  |
| 序號 | a | b | c | d | e | f |
| 實驗用品 | 溶液溫度 | 中和熱 | |||
| t1 | t2 | △H | |||
| ① | 50 mL 0.55 mol?L-1 NaOH溶液 | 50 mL 0.5 mol?L-1 HCl溶液 | 20℃ | 23.3℃ | |
| ② | 50 mL 0.55 mol?L-1 NaOH溶液 | 50 mL 0.5 mol?L-1 HCl溶液 | 20℃ | 23.5℃ | |
查看答案和解析>>
科目:高中化學 來源: 題型:
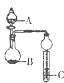
| A、若A為醋酸,B為貝殼,C中盛CaCl2溶液,則C中溶液變渾濁 |
| B、若A為濃硫酸,B為木炭,C中盛有硅酸鈉溶液,則C中出現白色渾濁 |
| C、若A為濃鹽酸,B為MnO2,C中盛石蕊試液,則C中溶液先變紅后褪色 |
| D、若A為濃氨水,B為生石灰,C中盛AlCl3溶液,則C中先產生白色沉淀后沉淀不溶解 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、此法的優點之一是原料來源豐富 |
| B、進行①②③步驟的目的是從海水中提取氯化鎂 |
| C、第④步電解制鎂是由于鎂是很活潑的金屬 |
| D、以上制取鎂的過程中涉及的反應有分解反應、化合反應和置換反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com