
 ,最高價氧化物的化學式為:Cl2O7.
,最高價氧化物的化學式為:Cl2O7. .
. .
.分析 A、B、C、D、E、F是原子序數由小到大排列的六種短周期主族元素,其中A、B、C、E的原子序數之和為32,A是元素周期表中原子半徑最小的元素,則A為H元素;B、C左右相鄰,C、E位于同主族,設B的原子序數為x,則C原子序數為x+1,E原子序數為x+1+8,故1+x+x+1+x+1+8=32,解得x=7,故B為N元素,C為O元素,E為S元素,則F為Cl;A與D同主族,結合原子序數之和可知,D為Na元素;
(1)F為Cl元素,原子核外有3個電子層,各層電子數為2、8、7;最高價正價為+7;
(2)A與C按原子數目1:1組成的化合物H2O2;
(3)D和F組成化合物為NaCl,由鈉離子與氯離子構成,用Na原子、Cl原子電子式表示其形成過程;
(4)由H、N、O、S四種元素中的三種組成的一種強酸,該強酸的稀溶液能與銅反應,則該酸為硝酸,稀硝酸與Cu反應方程式為:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;
(5)由H、N、O、S四種元素組成的一種離子化合物X,1molX能與足量NaOH濃溶液反應生成標準狀況下44.8L氣體,說明該物質陽離子為NH4+,且1molA中含有2molNH4+,則A為硫酸銨或亞硫酸銨,銨根離子與氫氧根離子反應生成氨氣;
(6)由H、N、O、S和Fe五種元素組成的式量為392的化合物Y,Y的溶液加入過量濃NaOH溶液并加熱,產生白色沉淀和無色刺激性氣味氣體,過一段時間白色沉淀變為灰綠色,最終變為紅褐色,可知Y中含有Fe2+、NH4+,另取B的溶液,加入過量BaCl2溶液產生白色沉淀,加鹽酸沉淀不溶解,則B中含有硫酸根離子,又1mol B中含有6mol結晶水,令Y的化學式為x(NH4)2SO4•yFeSO4•6H2O,結合其相對分子質量確定.
解答 解:A、B、C、D、E、F是原子序數由小到大排列的六種短周期主族元素,其中A、B、C、E的原子序數之和為32,A是元素周期表中原子半徑最小的元素,則A為H元素;B、C左右相鄰,C、E位于同主族,設B的原子序數為x,則C原子序數為x+1,E原子序數為x+1+8,故1+x+x+1+x+1+8=32,解得x=7,故B為N元素,C為O元素,E為S元素,則F為Cl;A與D同主族,結合原子序數可知,則D為Na元素;
(1)F為Cl元素,原子核外有3個電子層,各層電子數為2、8、7,原子結構示意圖為 ;最高價正價為+7,最高價氧化物化學式為:Cl2O7,
;最高價正價為+7,最高價氧化物化學式為:Cl2O7,
故答案為: ;Cl2O7;
;Cl2O7;
(2)A與C按原子數目1:1組成的化合物H2O2,電子式為: ,
,
故答案為: ;
;
(3)D和F組成化合物為NaCl,由鈉離子與氯離子構成,用電子式表示其形成過程為 ,
,
故答案為: ;
;
(4)由H、N、O、S四種元素中的三種組成的一種強酸,該強酸的稀溶液能與銅反應,則該酸為硝酸,稀硝酸與Cu反應方程式為:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,其中起酸性作用的酸占消耗酸總物質的量的百分比是$\frac{6}{8}$×100%=75%,
故答案為:75%;
(5)由H、N、O、S四種元素組成的一種離子化合物X,1molX能與足量NaOH濃溶液反應生成標準狀況下44.8L氣體,說明該物質陽離子為NH4+,且1molA中含有2molNH4+,則A為硫酸銨或亞硫酸銨,銨根離子與氫氧根離子反應生成氨氣,反應離子方程式為:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O,
故答案為:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O;
(6)①由H、N、O、S和Fe五種元素組成的式量為392的化合物Y,Y的溶液加入過量濃NaOH溶液并加熱,產生白色沉淀和無色刺激性氣味氣體.過一段時間白色沉淀變為灰綠色,最終變為紅褐色,可知Y中含有Fe2+、NH4+;
另取B的溶液,加入過量BaCl2溶液產生白色沉淀,加鹽酸沉淀不溶解,則B中含有硫酸根離子,又1mol B中含有6mol結晶水,令Y的化學式為x(NH4)2SO4•yFeSO4•6H2O,則:(96+36)x+(96+56)y+108=392,則x=y=1,故Y化學式為:(NH4)2SO4•FeSO4•6H2O,
②與足量Ba(OH)2溶液反應的離子方程式為:2NH4++Fe2++2SO42-+2Ba2++4OH-═Fe(OH)2↓+2BaSO4↓+2NH3↑+2H2O,
故答案為:(NH4)2SO4•FeSO4•6H2O;2NH4++Fe2++2SO42-+2Ba2++4OH-═Fe(OH)2↓+2BaSO4↓+2NH3↑+2H2O.
點評 本題考查位置結構性質的應用、無機物推斷等,明確B、C、E的位置及原子序數的關系來推斷元素是關鍵,需要學生熟練掌握元素化合物性質,難度較大.


 智趣寒假作業云南科技出版社系列答案
智趣寒假作業云南科技出版社系列答案科目:高中化學 來源: 題型:選擇題
| A. | 乙醛 | B. | 甲醛 | C. | 丙醛 | D. | 丁醛 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{1.225a}{35.5}$×100% | B. | $\frac{122.5(1-\frac{74.5×a%}{35.5})}{48}$×100% | ||
| C. | $\frac{1.225a}{35.5}$% | D. | 無法計算 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol苯乙烯中含有的碳碳雙鍵數為4NA | |
| B. | 0.1mol甲基中含有的電子數為NA | |
| C. | 2.8 g乙烯和聚乙烯的混合物中所含碳原子數為0.2NA | |
| D. | 標準狀況下,2.24LCHCl3含有的分子數為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 反應N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在溫度為T1、T2時,平衡體系中NO2的體積分數隨壓強的變化曲線如圖所示.下列說法正確的( )
反應N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在溫度為T1、T2時,平衡體系中NO2的體積分數隨壓強的變化曲線如圖所示.下列說法正確的( )| A. | a、c兩點的反應速率:a>c | |
| B. | a、c兩點氣體的顏色:a深,c淺 | |
| C. | b、c兩點的平衡常數:b<c | |
| D. | a、c兩點氣體的平均相對分子質量:a>c |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH2=CH2 | B. | C6H5OH | C. | 裂化汽油 | D. | 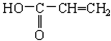 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 物質 | 使用的試劑 | 主要操作 |
| A | 乙醇(水) | 金屬鈉 | 過濾 |
| B | 乙酸乙酯(乙酸) | 飽和碳酸鈉溶液 | 振蕩、分液 |
| C | 苯(苯酚) | 濃溴水 | 過濾 |
| D | 乙烷(乙烯) | 酸性高錳酸鉀溶液 | 洗氣 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.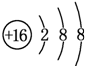 ;D與E能形成一種結構類似于CO2的三原子分子,且每個原子均達到了8e-穩定結構,該分子的結構式為S=C=S,電子式為
;D與E能形成一種結構類似于CO2的三原子分子,且每個原子均達到了8e-穩定結構,該分子的結構式為S=C=S,電子式為 ,化學鍵類型為極性共價鍵(填“離子鍵”、“非極性共價鍵”或“極性共價鍵”).
,化學鍵類型為極性共價鍵(填“離子鍵”、“非極性共價鍵”或“極性共價鍵”).查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com