
| A. | S(g)+O2(g)═SO2(g)△H1;S(s)+O2═SO2(g)△H2,則△H1>△H2 | |
| B. | C(石墨,s)═C(金剛石,s)△H=+1.9kJ•mol-1,則金剛石比石墨穩定 | |
| C. | OH-(aq)+H+(aq)=H2O(l)△H=-57.4kJ•mol-1,則:含20gNaOH的稀溶液與過量稀醋酸完全反應,放出的熱量為28.7kJ | |
| D. | 2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1,則碳的燃燒熱大于110.5kJ•mol-1 |
分析 A.固體硫燃燒時要先變為氣態硫,過程吸熱,據此確定反應熱的大小;
B.物質的能量越高越不穩定;
C.反應過程中,稀醋酸電離要吸熱;
D.1mol可燃物完全燃燒生成穩定的氧化物放出的熱量為燃燒熱.
解答 解:A.固體硫燃燒時要先變為氣態硫,過程吸熱,氣體與氣體反應生成氣體比固體和氣體反應生成氣體產生熱量多,但反應熱為負值,所以△H1<△H2;故A錯誤;
B.C(石墨,S)=C(金剛石,S)△H=+l.9 kJ/mol,則由石墨制取金剛石的反應是吸熱反應,金剛石的能量比石墨高,則石墨比金剛石穩定,故B錯誤;
C.OH-(aq)+H+(aq)=H2O(l)△H=-57.4kJ•mol-1,但由于稀醋酸電離要吸熱,所以含20gNaOH的稀溶液與過量稀醋酸完全反應,放出的熱量小于28.7kJ,故C錯誤;
D.2C(s)+O2(g)=2CO(g)△H=-221kJ/mol,該反應方程式中C的物質的量為2mol,生成的氧化物為CO不是穩定氧化物,還會繼續燃燒放熱,所以碳的燃燒熱大于110.5kJ•mol-1,故D正確.
故選D.
點評 本題考查了反應熱大小比較、中和熱、燃燒熱等,側重于基礎知識的考查,題目難度不大,注意把握燃燒熱和中和熱的概念.


 同步拓展閱讀系列答案
同步拓展閱讀系列答案科目:高中化學 來源: 題型:選擇題
| A. | 凡可燃性氣體點燃時都要先檢驗純度 | |
| B. | 某物質在空氣中燃燒生成二氧化碳和水,該物質一定為甲烷 | |
| C. | 沼氣、天然氣、煤氣的主要成份都是甲烷 | |
| D. | 甲烷和氫氣一樣也是一種最理想的氣體燃料 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 45.5% | B. | 68.0% | C. | 75.4% | D. | 無法計算 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 攪拌能加快蔗糖在水中的溶解,其原因是增大了蔗糖的溶解度 | |
| B. | 天氣悶熱時,魚塘的魚會接近水面游動,原因是溫度高壓強小,氧氣的溶解度小 | |
| C. | 夏天,銅制眼鏡架表面出現的綠色物質[主要成分 Cu2(OH)2CO3],可用稀鹽酸除去 | |
| D. | 敞口放置的酒精沒有燃燒的原因是溫度沒有達到酒精的著火點 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

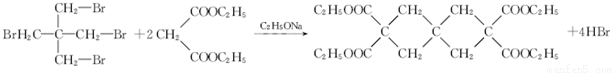
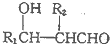 (R1、R2為烴基或H)
(R1、R2為烴基或H)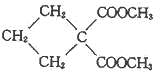 +HBr+HCl
+HBr+HCl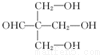 .
. .
.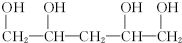 .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標況下,1mol的NH3 | B. | 4℃時,18克水 | ||
| C. | 2mol的Al(密度為2.7g•cm-3) | D. | 常溫常壓下1mol的CO2氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 小于$\frac{1}{2}$ | B. | 大于$\frac{1}{2}$,小于1 | C. | 等于$\frac{1}{2}$ | D. | 大于1,小于2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com