
| 操作及現象 | 結論 | |
| A | 向AgCl懸濁液中加入NaI溶液時出現黃色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| B | 向某溶液中滴加氯水后再加入KSCN溶液,溶液呈紅色 | 溶液中一定含有Fe2+ |
| C | 向NaBr溶液中滴入少量氯水和苯,振蕩、靜置,溶液上層呈橙紅色 | Br-還原性強于Cl- |
| D | 加熱盛有NH4Cl固體的試管,試管底部固體消失,試管口有晶體凝結 | NH4Cl固體可以升華 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.同類型的沉淀轉化時,溶度積大的沉淀轉化為溶度積小的沉淀;
B.原溶液中含有Fe3+,加入KSCN溶液,溶液呈紅色;
C.向NaBr溶液中滴入少量氯水和苯,振蕩、靜置,溶液上層呈橙紅色,說明有Br2生成,發生反應:2Br-+Cl2=2Cl-+Br2,還原劑還原性強于還原產物還原性;
D.NH4Cl受熱分解為NH3與HCl,在試管口處冷卻,NH3與HCl反應又得到NH4Cl固體.
解答 解:A.同類型的沉淀轉化時,難溶電解質之間可實現由溶度積常數較大的物質轉化為溶度積常數較小的物質,AgCl懸濁液中加入KI溶液,白色沉淀變成黃色,證明此條件下Ksp(AgCl)>Ksp(AgI),故A錯誤;
B.原溶液中若含有Fe3+,加入KSCN溶液,溶液也會呈紅色,不能說明原溶液中是否含有Fe2+,故B錯誤;
C.向NaBr溶液中滴入少量氯水和苯,振蕩、靜置,溶液上層呈橙紅色,說明有Br2生成,發生反應:2Br-+Cl2=2Cl-+Br2,說明Br-還原性強于Cl-,故C正確;
D.NH4Cl受熱分解為NH3與HCl,在試管口處冷卻,NH3與HCl反應又得到NH4Cl固體,不能說明NH4Cl固體可以升華,故D錯誤,
故選:C.
點評 本題考查化學實驗方案評價,側重考查學生對基礎知識的理解掌握,難度不大.


科目:高中化學 來源: 題型:解答題


| 物理量 實驗序號 | V(溶液)/ml | … | |||
| 1 | 100 | … | |||
| 2 | 100 | … |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 稀醋酸中加入少量醋酸鈉能增大醋酸的電離程度 | |
| B. | 25℃時,等體積等濃度的硝酸與氨水混合后,溶液pH=7 | |
| C. | 25℃時,0.1mol•L-1的硫化氫溶液比等濃度的硫化鈉溶液的導電能力弱 | |
| D. | 0.1mol AgCl和0.1molAgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| X | ||
| Y | Z | W |
| T |
| A. | X、W、Z元素的原子半徑及它們的氣態氫化物的熱穩定性均依次遞增 | |
| B. | Y、Z、W元素在自然界中均不能以游離態存在,它們的最高價氧化物的水化物的酸性依次遞增 | |
| C. | YX2晶體熔化、液態WX3氣化均需克服分子間作用力 | |
| D. | 根據元素周期律,可以推測T元素的單質具有半導體特性,T2X3具有氧化性和還原性 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| V(AgNO3)/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
| E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |


查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 都是平面型分子
都是平面型分子查看答案和解析>>
科目:高中化學 來源: 題型:解答題
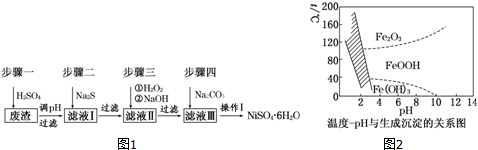
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
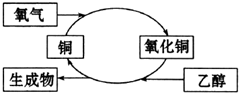
| A. | 生成物是乙醛 | B. | 乙醇發生了還原反應 | ||
| C. | 銅是此反應的催化劑 | D. | 反應中有紅黑顏色交替變化的現象 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 GTN{[Ni(CHZ)3](ClO4)2}是一種具有較強爆轟成長距離的初發藥.
GTN{[Ni(CHZ)3](ClO4)2}是一種具有較強爆轟成長距離的初發藥.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com