


分析 金屬A與水反應生成氣體甲和物質D,D的焰色反應為黃色證明A為Na,則甲為H2,D為NaOH;金屬B和氫氧化鈉溶液反應產(chǎn)生氫氣,說明B為Al,氣體甲和氯氣反應生成丙為HCl,物質E為鹽酸溶液,物質D氫氧化鈉和物質G為反應生成紅褐色沉淀H為Fe(OH)3,G為FeCl3,推斷物質F為FeCl2,判斷C為Fe,據(jù)此答題,
(1)根據(jù)上面的分析可知,B為Al,丙為HCl;
(2)氫氧化鈉為離子化合物,電子式中需要標出陰陽離子所帶電荷,氫氧根離子需要標出最外層電子;
(3)氫氣在Cl2中燃燒放出蒼白色火焰,生成易溶于水的氯化氫氣體;
(4)金屬A與G的水溶液反應是鈉和氯化鐵溶液的反應,鈉先和水反應生成氫氧化鈉和氫氣,氫氧化鈉和氯化鐵反應生成氫氧化鐵沉淀和氯化鈉;
(5)反應③是金屬鋁和氫氧化鈉溶液的反應生成偏鋁酸鈉和氫氣,據(jù)此書寫離子方程式.
解答 解:金屬A與水反應生成氣體甲和物質D,D的焰色反應為黃色證明A為Na,則甲為H2,D為NaOH;金屬B和氫氧化鈉溶液反應產(chǎn)生氫氣,說明B為Al,氣體甲和氯氣反應生成丙為HCl,物質E為鹽酸溶液,物質D氫氧化鈉和物質G為反應生成紅褐色沉淀H為Fe(OH)3,G為FeCl3,推斷物質F為FeCl2,判斷C為Fe,
(1)根據(jù)上面的分析可知,B為Al,丙為HCl,
故答案為:Al;HCl;
(2)氫氧化鈉屬于離子化合物,電子式中需要標出陰陽離子所帶電荷,鈉離子直接用離子符號表示,氫氧根離子需要標出最外層電子,氫氧化鈉的電子式為: ,
,
故答案為: :
:
(3)氫氣在Cl2中燃燒的現(xiàn)象為:有蒼白色火焰,瓶口有白霧,
故答案為:有蒼白色火焰,瓶口有白霧;
(4)金屬A與G的水溶液反應的化學方程式:6Na+2FeCl3+6H2O=2Fe(OH)3↓+6NaCl+3H2↑,
故答案為:6Na+2FeCl3+6H2O=2Fe(OH)3↓+6NaCl+3H2↑;
(5)反應③的離子方程式為2OH-+2H2O+2Al=2AlO2-+3H2↑,
故答案為:2OH-+2H2O+2Al=2AlO2-+3H2↑.
點評 本題考查無機物的推斷,注意把握焰色反應及物質的顏色為解答本題的突破口,熟悉物質的性質即可解答,題目難度中等.


 全能測控一本好卷系列答案
全能測控一本好卷系列答案科目:高中化學 來源: 題型:解答題

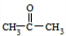 +2H2O;
+2H2O;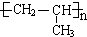 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子及其簡單陰離子的核外電子層數(shù)都等于該元素所在的周期數(shù) | |
| B. | 原子最外層電子數(shù)都等于其所在的族序數(shù) | |
| C. | 元素周期表從ⅢB到ⅡB族共8個縱行,全都是金屬元素 | |
| D. | 同周期表中ⅦA族元素的原子半徑較小 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | E | F | H | I | K | |||
| 3 | B | C | D | G | J |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 無色溶液中:Na+、Cl-、SO42-、Fe3+ | |
| B. | 在強酸性的溶液中:Na+、SO42-、Cl-、NH4+ | |
| C. | 使紫色石蕊試液變紅的溶液中:Na+、Mg2+、CO32-、Cl- | |
| D. | 含SO42-的水溶液中:K+、Ba2+、Cl-、Br- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | c(Na+)>c(HS-)>c(K+)>c(S2-)>c(OH-)>c(H+) | B. | c(H+)>c(OH-) | ||
| C. | 2 c(K+)+c(H+)=c(OH-)+c(HS-)+2 c(S2-) | D. | c(OH-)+c(S2-)=c(H+)+c(HS-)+2 c(H2S) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 漂白粉、次氯酸溶液和明礬都是混合物 | |
| B. | 不能通過化合反應制得FeCl2和Fe(OH)3 | |
| C. | 鐵能在氧氣中劇烈燃燒,但不能在水蒸氣中燃燒 | |
| D. | 用強光照射裝滿次氯酸的試管(倒置于水槽中)可收集到兩種氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 降低溫度,當A質量不變時,說明該反應已達平衡 | |
| B. | 若D為氣體,再加入1mol A,平衡正向移動,A的轉化率增大 | |
| C. | 升高溫度,正反應的平衡常數(shù)增大 | |
| D. | 若D為固體,再加入1mol A,平衡不移動,A在混合氣體中的百分含量不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
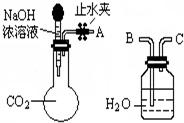 純堿、燒堿等是重要的化工原料.
純堿、燒堿等是重要的化工原料.| 實驗步驟 | 預期現(xiàn)象和結論 |
| 步驟1: | |
| 步驟2: |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com