
| A. | 0.01molMg在空氣中完全燃燒生成MgO和Mg3N2,轉移電子數目為0.02NA | |
| B. | 常溫常壓下,18.00克重水(D2O)中所含電子數約為10NA | |
| C. | 在熔融狀態下1molNaHSO4所含陽離子數為2NA | |
| D. | 1mol FeCl3完全水解轉化為氫氧化鐵膠體后能生成NA個膠粒 |
分析 A、根據反應后無論生成何種產物,鎂元素的化合價均變為+2價來分析;
B、求出重水的物質的量,然后根據1mol重水中含10mol電子來分析;
C、NaHSO4在熔融狀態下只能電離出鈉離子和HSO4-;
D、一個氫氧化鐵膠粒是多個氫氧化鐵分子的聚集體.
解答 解:A、反應后無論生成何種產物,鎂元素的化合價均變為+2價,即1mol鎂轉移2mol電子,則0.01mol鎂轉移0.01mol電子,與產物無關,故A正確;
B、18g重水的物質的量n=$\frac{18g}{20g/mol}$=0.9mol,而1mol重水中含10mol電子,故0.9mol重水中含9mol電子即9NA個,故B錯誤;
C、由于共價鍵在熔融狀態不能斷裂,故NaHSO4在熔融狀態下只能電離出鈉離子和HSO4-,即1molNaHSO4在熔融狀態下只能電離出2mol離子即2NA個,故C錯誤;
D、一個氫氧化鐵膠粒是多個氫氧化鐵分子的聚集體,故1mol氯化鐵轉化得到的氫氧化鐵膠粒的個數小于NA個,故D錯誤.
故選A.
點評 本題考查了阿伏伽德羅常數數的有關計算,掌握公式的應用和物質的結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:解答題
| 轉化率(%) | 0.1MPa | 0.5MPa | 1.0MPa | 10MPa |
| 400℃ | 99.2% | 99.6% | 99.7% | 99.9% |
| 500℃ | 93.5% | 96.9% | 97.8% | 99.3% |
| 600℃ | 73.7% | 85.8% | 89.5% | 96.4% |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
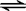 CH3COOH+OH-;
CH3COOH+OH-;查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某銨態氮肥由W、X、Y、Z 4種短周期元素組成,其中W的原子半徑最小.
某銨態氮肥由W、X、Y、Z 4種短周期元素組成,其中W的原子半徑最小. ;
; ;
;查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 pC是指極稀溶液中溶質物質的量濃度的常用對數負值,類似pH.如某溶液溶質的濃度為1×10-3 mol•L-1,則該溶液中該溶質的pC=-lg10-3=3.已知H2CO3溶液中存在下列平衡:CO2+H2O?H2CO3 H2CO3?H++HCO3- HCO3-?H++CO32-.如圖為H2CO3、HCO3-、CO32-在加入強酸或強堿溶液后,達到平衡時溶液中三種成分的pCpH圖.
pC是指極稀溶液中溶質物質的量濃度的常用對數負值,類似pH.如某溶液溶質的濃度為1×10-3 mol•L-1,則該溶液中該溶質的pC=-lg10-3=3.已知H2CO3溶液中存在下列平衡:CO2+H2O?H2CO3 H2CO3?H++HCO3- HCO3-?H++CO32-.如圖為H2CO3、HCO3-、CO32-在加入強酸或強堿溶液后,達到平衡時溶液中三種成分的pCpH圖. H++HCO3-平衡向左移動放出CO2,碳酸濃度保持不變.
H++HCO3-平衡向左移動放出CO2,碳酸濃度保持不變.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 反應停止了 | B. | 正反應速率與逆反應速率相等 | ||
| C. | 反應物和生成物濃度相等 | D. | 正反應速率與逆反應速率均為零 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NO是一種紅棕色氣體,易溶于水 | |
| B. | 汽車尾氣中NO的來源是空氣中的N2與O2在汽車氣缸內的高溫環境下的反應產物 | |
| C. | 工業生產硝酸的原料主要有NO和空氣 | |
| D. | 由于NO在血管中的特殊作用,所以NO無毒 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | HA溶液的導電性較弱,則HA為弱酸 | |
| B. | S02的水溶液能導電,則S02為電解質 | |
| C. | HC1在水中能完全電離,則鹽酸為強電解質 | |
| D. | BaS04是電解質,但其水溶液不導電 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaHS水解:HS-+H2O?S2-+H3O+ | |
| B. | 向硫酸鐵溶液中加入鐵:Fe3++Fe═2Fe2+ | |
| C. | 在鐵上鍍銅陽極反應為:Cu2++2e-═Cu | |
| D. | 氯化銅水解:Cu2++2H2O?Cu(OH)2+2H+ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com