
| A. | 6.8g液態KHSO4中含有0.1NA個陽離子 | |
| B. | 18g D2O和18g H2O中含有的質子數均為10NA | |
| C. | $\frac{1}{18}$mol的H37Cl分子所含中子數為NA | |
| D. | 過氧化鈉與水反應時,生成0.1mol氧氣轉移的電子數為0.2NA |
分析 A、求出KHSO4的物質的量,然后根據液態KHSO4能電離出鉀離子和硫酸氫根離子來分析;
B、重水的摩爾質量為20g/mol;
C、H37Cl中20個中子;
D、過氧化鈉和水反應時,氧元素由-1價變為0價來分析.
解答 解:A、6.8gKHSO4的物質的量為0.05mol,而液態KHSO4能電離出鉀離子和硫酸氫根離子,故0.05mol硫酸氫鉀中含0.05NA個陽離子,故A錯誤;
B、重水的摩爾質量為20g/mol,故18g重水的物質的量為0.9mol,故含9NA個質子,故B錯誤;
C、H37Cl中20個中子,故$\frac{1}{18}$mol的H37Cl中含$\frac{10}{9}$NA個中子,故C錯誤;
D、過氧化鈉和水反應時,氧元素由-1價變為0價,故當生成0.1mol氧氣時轉移0.2NA個電子,故D正確.
故選D.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化學反應伴隨能量變化,是化學反應的基本特征之一 | |
| B. | 常溫下,氫氧化鋇晶體與氯化銨晶體混合放出氨氣,該反應為放熱反應 | |
| C. | 化學反應中能量變化的大小與反應物的質量多少無關 | |
| D. | 舊化學鍵斷裂所放出的能量高于新化學鍵形成所吸收的能量時發生放熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 工業上通過將空氣冷凝成液體后再分離的方式獲得液氧 | |
| B. | 推進劑燃燒后的主要產物是水和二氧化碳 | |
| C. | 煤油屬于純凈物,主要成分是烴 | |
| D. | 氧氣與煤油的反應是放熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
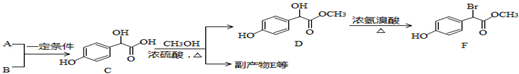
 ;
;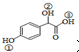 )中①、②、③3個-OH的酸性由強到弱的順序是③>①>②;
)中①、②、③3個-OH的酸性由強到弱的順序是③>①>②; .
.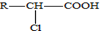 .A有多種合成方法,請寫出由乙酸合成A的路線流程圖(其他原料任選),合成路線流程圖示例如下:H2C=CH2$→_{催化劑,△}^{H_{2}}$CH3CH2OH$→_{濃硫酸,△}^{CH_{3}COOH}$CH3COOC2H5.
.A有多種合成方法,請寫出由乙酸合成A的路線流程圖(其他原料任選),合成路線流程圖示例如下:H2C=CH2$→_{催化劑,△}^{H_{2}}$CH3CH2OH$→_{濃硫酸,△}^{CH_{3}COOH}$CH3COOC2H5.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ① | B. | ② | C. | ③ | D. | ④ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com