
| A. | CO(g)的燃燒熱是283.0 kJ/mol,則表示CO燃燒熱的熱化學方程式為2CO(g)+O2(g)═2CO2(g);△H=-566.0 kJ/mol | |
| B. | 由石墨比金剛石穩定可知:C(金剛石,s)=C(石墨,s);△H<0 | |
| C. | 需要加熱才能發生的反應一定是吸熱反應 | |
| D. | 已知:2SO2 (g)+O2(g)?2SO3 (g);△H=-98.3 kJ/mol.將1 mol SO2和0.5 mol O2充入一密閉容器中反應,放出49.15 kJ的熱量 |
分析 A.燃燒熱的熱化學方程式中,可燃物的物質的量必須為1mol,即CO的系數必須為1;
B.物質具有的能量越高,物質的穩定性越弱,結合該反應為放熱反應分析;
C.反應條件與反應熱沒有必然關系,則需要加熱才能發生的反應不一定是吸熱反應;
D.該反應為可逆反應,反應物不可能完全轉化成生成物,則反應放出熱量減少.
解答 解:A.燃燒熱是指1mol可燃物完全燃燒生成穩定的氧化物放出的熱量,表示CO(g)燃燒熱的熱化學方程式為CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283.0KJ/mol,故A錯誤;
B.根據反應C(金剛石,s)=C(石墨,s)△H<0可知,該反應為放熱反應,說明金剛石具有的能量大于金剛石,則石墨比金剛石穩定,故B正確;
C.需要加熱才能發生的反應不一定是吸熱反應,如鋁熱反應、氫氣還原氧化銅等反應都是放熱反應,但是該反應需要在加熱條件下進行,故C錯誤;
D.已知:2SO2 (g)+O2(g)?2SO3 (g)△H=-98.3 kJ/mol,說明2mol二氧化硫完全轉化成2mol三氧化硫放出98.3kJ熱量;若將1 mol SO2和0.5 mol O2充入一密閉容器中反應,由于該反應為可逆反應,則反應生成三氧化硫的物質的量一定小于1mol,反應放出熱量一定小于98.3 kJ/mol×$\frac{1mol}{2mol}$=49.15 kJ,故D錯誤;
故選B.
點評 本題考查熱化學方程式的書寫及應用,題目難度中等,明確燃燒熱概念、可逆反應特點為解答關鍵,B為易錯點,注意掌握物質穩定性與物質具有能量的關系,試題側重考查學生的靈活應用能力.


科目:高中化學 來源: 題型:選擇題
| A. | Ba(OH)2溶液中加入過量Al2(SO4)3溶液:3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)3↓ | |
| B. | FeCl3溶液中加少量Na2S溶液:2Fe3++S2-=2Fe2++S↓ | |
| C. | 向硫酸銅溶液中加入過量氨水:Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+ | |
| D. | 向Ca(OH)2溶液中加入過量的NaHCO3溶液:Ca2++2HCO3-+2OH-=CO32-+CaCO3↓+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | OH-的電子式: | |
| B. | F-的結構示意圖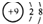 | |
| C. | N2的結構式: | |
| D. | 碳酸氫鈉的電離方程式:NaHCO3=Na++H++CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 序號 | 反應① | 反應② |
| A | 向AgNO3溶液中滴加稀鹽酸 | AgNO3溶液與食鹽水混合 |
| B | 過量CO2通入NaOH溶液中 | 過量CO2通入澄清石灰水中 |
| C | 向燒堿溶液中滴加稀鹽酸 | 向H2SO4溶液中滴加KOH溶液 |
| D | 向BaCl2溶液中滴加稀硫酸 | 向Ba(OH)2溶液中滴加CuSO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 碳碳雙鍵
碳碳雙鍵 3-甲基-2-乙基-1-戊烯④
3-甲基-2-乙基-1-戊烯④ 2-甲基戊烷
2-甲基戊烷 +3HNO3$→_{△}^{濃硫酸}$
+3HNO3$→_{△}^{濃硫酸}$ +3H2O.
+3H2O.查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
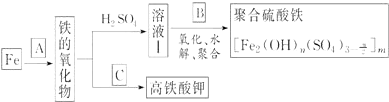
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1說明2molH2(g)和1molO2(g)的能量總和小于2molH2O(g)的能量 | |
| B. | 已知C(石墨,s)=C(金剛石,s);△H>0,則金剛石比石墨穩定 | |
| C. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4kJ•mol-1,則含20gNaOH的稀溶液與稀鹽酸完全中和,放出28.7kJ的熱量 | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1; 2C(s)+O2(g)=2CO(g)△H2;則△H1>△H2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol Cl2與常溫下氫氧化鈉溶液充分反應時轉移的電子數為2NA | |
| B. | 1molCu與足量的硫固體反應轉移的電子數為NA | |
| C. | 常溫下,1 L 0.1 mol/L MgCl2溶液中含Mg2+數為0.1NA | |
| D. | 標準狀況下,2.24L三氧化硫所含分子數為0.1 NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com