
分析 相同條件下,氣體體積之比等于物質的量之比,根據n=$\frac{m}{M}$計算二者物質的量之比,再根據$\overline{M}$=$\frac{{m}_{總}}{{n}_{總}}$計算平均相對分子質量.
解答 解:相同條件下,體積比為1:2的H2和O2的物質的量之比為1:2,則平均相對分子質量為$\frac{1×2+2×32}{1+2}$=22;
質量比為1:2的H2和O2的物質的量之比為$\frac{1}{2}$:$\frac{2}{32}$=8:1,則平均相對分子質量為$\frac{8×2+32×1}{8+1}$=5.33,
故答案為:22;5.33.
點評 本題考查物質的量有關計算,比較基礎,注意對公式的理解與靈活應用.


科目:高中化學 來源: 題型:解答題
| 陽離子 | H+、Na+、A13+、Ag+、Ba2+ |
| 陰離子 | OH-、C1-、CO32-、NO3-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
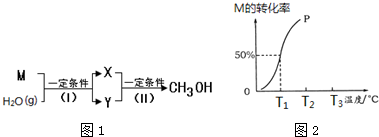
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 質量守恒、電子守恒、電荷守恒 | B. | 電子守恒、質量守恒、電荷守恒 | ||
| C. | 電子守恒、電荷守恒、質量守恒 | D. | 電荷守恒、質量守恒、電子守恒 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在1 min時:c(SO3)+c(SO2)=1.0mol/L | |
| B. | 2 min 內:v(SO2)=0.25mol/(L•min) | |
| C. | 若再充入2mol SO3,達平衡時SO3%(質量分數)減小 | |
| D. | 反應條件相同,若起始時向反應容器中充入2mol SO3,平衡時反應吸熱0.75a kJ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 冶煉鎂的最后一步反應為電解MgCl2溶液 | |
| B. | 由氯化鎂的結晶水合物得到氯化鎂屬于物理變化 | |
| C. | 利用海水和石灰水作用可以得到氯化鎂 | |
| D. | 利用氯化鎂冶煉金屬鎂而不利用氧化鎂的原因是氧化鎂的熔點太高 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 石油和天然氣的主要成分都是碳氫化合物 | |
| B. | 乙醇、乙酸和乙酸乙酯可以用飽和碳酸鈉溶液鑒別 | |
| C. | 在酸性條件下,CH3CO18OC2H5的水解產物是CH3CO18OH和C2H5OH | |
| D. | 甘氨酸(NH2-CH2-COOH)既能與NaOH反應,又能與鹽酸反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com