
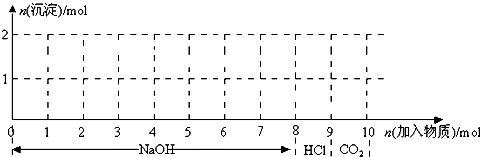
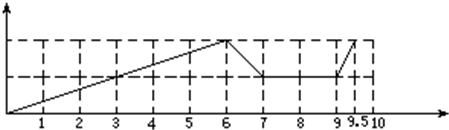
(7分)現有含1mol Fe3+和1molAl3+的混合溶液,按下圖橫坐標依次加入NaOH溶液、鹽酸、通入CO2氣體,縱坐標為混合沉淀的物質的量。
(1)請畫出沉淀的物質的量隨反應的變化曲線

(2)逐步寫出:6-7、9-10反應的離子方程式:____________________________________。
(1)(4分)
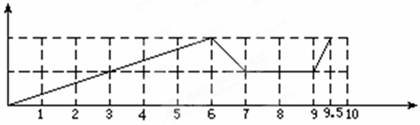
(2)Al(OH)3+OH-=AlO2-+2H2O;
CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32- CO2+ CO32-+H2O=2HCO3-
【解析】根據試劑可知,反應的方程式先后為Fe3++3OH-=Fe(OH)3、Al3++3OH-=Al(OH)3,此時消耗氫氧化鈉是6mol。則繼續加入氫氧化鈉,氫氧化鋁溶解,方程式為Al(OH)3+OH-=AlO2-+2H2O。所以此時加入的2mol氫氧化鈉,剩余1mol。因此加入鹽酸,首先中和剩余的氫氧化鈉,需要1mol鹽酸。如果此時通入CO2,則CO2和偏鋁酸鈉反應生成氫氧化鋁沉淀,方程式為CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-,消耗CO2是0.5mol。則另外0.5molCO2和生成的碳酸鈉反應,生成碳酸氫鈉,方程式為CO2+ CO32-+H2O=2HCO3-。


科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源:2013屆江西省南昌二中高三第一次考試化學試卷(帶解析) 題型:填空題
(7分)現有含1mol Fe3+和1molAl3+的混合溶液,按下圖橫坐標依次加入NaOH溶液、鹽酸、通入CO2氣體,縱坐標為混合沉淀的物質的量。
(1)請畫出沉淀的物質的量隨反應的變化曲線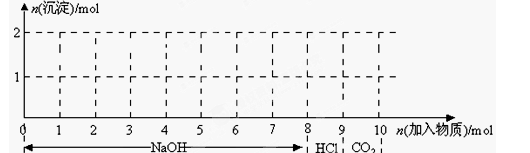
(2)逐步寫出:6-7、9-10反應的離子方程式:____________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:
現有含1mol Fe3+和1molAl3+的混合溶液,按下圖橫坐標依次加入NaOH溶液、
鹽酸、通入CO2氣體,縱坐標為混合沉淀的物質的量。
(1)請畫出沉淀的物質的量隨反應的變化曲線

(2)逐步寫出:6-7、9-10反應的離子方程式:____________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com