
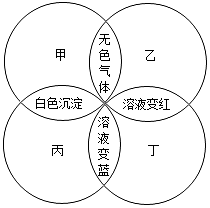
 甲、乙、丙、丁分別是石蕊溶液、稀硫酸、碳酸鈉溶液、澄清石灰水中的一種,若用四個圓表示四種溶液,兩圓相交部分為兩溶液混合后出現的主要實驗現象,如圖所示.請回答:
甲、乙、丙、丁分別是石蕊溶液、稀硫酸、碳酸鈉溶液、澄清石灰水中的一種,若用四個圓表示四種溶液,兩圓相交部分為兩溶液混合后出現的主要實驗現象,如圖所示.請回答:分析 (1)根據石蕊溶液是酸堿指示劑,遇到酸和堿呈現不同的顏色考慮本題;
(2)根據方程式的寫法和復分解反應的特點考慮.
解答 解:(1)由于石蕊溶液是酸堿指示劑,遇到酸變成紅色,遇到堿變成藍色,再根據圖示中丁與乙結合呈現紅色,丁與丙結合呈現藍色,所以丁是酸堿指示劑石蕊試液,所以乙是稀硫酸,因為硫酸與碳酸鈉反應生成硫酸鈉、水、二氧化碳,所以甲是碳酸鈉溶液,丙就是氫氧化鈣溶液,石蕊溶液是酸堿指示劑,遇到酸和堿呈現不同的顏色,可以用來判斷溶液的酸堿性,
故答案為:石蕊溶液;判斷溶液的酸堿性;
(2)由上面的推斷可知甲是碳酸鈉,丙是氫氧化鈣,所以該反應的反應物是碳酸鈉和氫氧化鈣,生成物是碳酸鈣沉淀和氫氧化鈉,離子方程式為:CO32-+Ca2+═CaCO3↓,用觀察法配平,碳酸鈣后面標上沉淀符號;兩種化合物相互交換成分生成兩種新的化合物的反應,屬于復分解反應,該反應符合這一特點,屬于復分解反應.
故答案為:CO32-+Ca2+═CaCO3↓;復分解反應.
點評 解答本題關鍵是要知道石蕊溶液遇到酸變紅色,遇到堿變藍色;要熟悉方程式的寫法和復分解反應的特點.


科目:高中化學 來源: 題型:選擇題
| A. | 道爾頓提出原子學說,門捷列夫發現元素周期律 | |
| B. | 化學研究的主要目的就是認識分子 | |
| C. | 研究物質的性質,常常運用觀察、實驗、分類、比較等方法 | |
| D. | 化學家可以在微觀層面上操縱分子和原子,組裝分子材料、分子器件和分子機器 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 如圖為實驗室某濃硫酸試劑瓶上的標簽,試根據有關數據回答下列問題:
如圖為實驗室某濃硫酸試劑瓶上的標簽,試根據有關數據回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.3molHNO3 | B. | 0.2molH3PO4 | ||
| C. | 3.01×1023個HNO3分子 | D. | 0.1molNH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 編號 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 名稱 | 酒精 | 醋酸 | 火堿 | 食鹽 | 銅導線 | 亞硫酸酐 | 蘇打 |
| 主要成分 | CH3CH2OH | CH3COOH | NaOH | NaCl | Cu | SO2 | Na2CO3 |
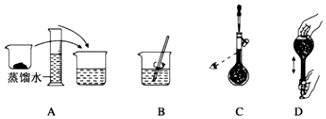
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 (1)已知如圖所示的可逆反應:
(1)已知如圖所示的可逆反應:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com