
分析 (1)溶液的pH=2.0,則c(OH-)=10-12mol/L,根據Ksp[Fe(OH)3]=c(Fe3+)×c3(OH-)計算;
(2)步驟3若未除去Fe3+,則加KI固體時,先發生2Fe3++2I-═2Fe2++I2,后發生2Cu2++4I-═2CuI↓+I2,反應消耗的碘離子的物質的量偏大;
(3)設Cu2S和CuS的物質的最分別為x、y,根據2Cu2+~I2~2S2O32-,利用原子守恒列式求出Cu2S和CuS的物質的量、質量,再求出質量分數.
解答 解:(1)步驟3加入氨水產生沉淀時,溶液的pH=2.0,則c(OH-)=10-12mol/L,Ksp[Fe(OH)3]=c(Fe3+)×c3(OH-),則c(Fe3+)=$\frac{2.6×1{0}^{-39}}{{c}^{3}(O{H}^{-})}$=2.6×10-3 mol•L-1,
故答案為:2.6×10-3mol•L-1;
(2)步驟3若未除去Fe3+,則加KI固體時,先發生2Fe3++2I-═2Fe2++I2,后發生2Cu2++4I-═2CuI↓+I2,反應消耗的碘離子的物質的量偏大,所以求出的Cu2+的物質的量將偏高,
故答案為:偏高;
(3)設Cu2S和CuS的物質的最分別為x、y,
根據關系式2Cu2+~I2~2S2O32-可知:n(Cu2+)=n(S2O32-)=0.050 00 mol•L-1×14.00×10-3 L=7.000×10-4 mol,
則:2x+y=7.000×10-4 mol×$\frac{250mL}{25mL}$…①,
Cu2S和CuS被高錳酸鉀氧化為CuSO4,Cu、S元素失去電子的物質的量等于Mn元素得到電子的物質的量,
則10x+8y=0.120 0mol•L-1×0.1L×5-0.100mol•L-1×0.016L×$\frac{250mL}{25mL}$…②,
聯立方程式①②,
解得:x=2.000×10-3mol、y=3.000×10-3mol,
試樣中Cu2S的質量分數為:w(Cu2S)=$\frac{2.000×1{0}^{-3}mol×160g/mol}{0.7500g}$×100%=42.7%,
試樣中CuS的質量分數為:w(CuS)=$\frac{3.000×1{0}^{-3}mol×96g/mol}{0.7500g}$×100%=38.4%,
答:Cu2S的質量分數為42.7%,CuS的質量分數為38.4%.
點評 本題考查了物質組成分析與化學綜合計算題,涉及氧化還原反應滴定、溶度積的計算等,難度中等,注意運用元素守恒進行推理計算,學習中緊緊抓住元素守恒、質量守恒、電荷守恒、極端分析等化學常用分析方法.


科目:高中化學 來源: 題型:解答題
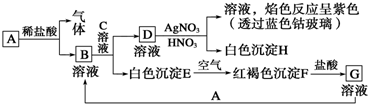
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 中性、漂白性 | B. | 酸性、漂白性 | C. | 只有酸性 | D. | 只有漂白性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 堿金屬單質的熔點隨原子序數的增大而降低 | |
| B. | Cs是第ⅠA族元素,Cs失電子能力比Na的強 | |
| C. | 砹(At)是第VIIA族,其氫化物的穩定性大于HCl | |
| D. | 第三周期金屬元素的最高價氧化物對應水化物,其堿性隨原子序數的增大而減弱 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| X | Y | |
| Z | W |
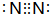 ;Y和氫元素形成的10電子微粒中常見的+1價陽離子為H3O+(填化學式,下同);Z和氫元素形成的18電子微粒中常見的-1價陰離子為HS-;
;Y和氫元素形成的10電子微粒中常見的+1價陽離子為H3O+(填化學式,下同);Z和氫元素形成的18電子微粒中常見的-1價陰離子為HS-;查看答案和解析>>
科目:高中化學 來源: 題型:填空題
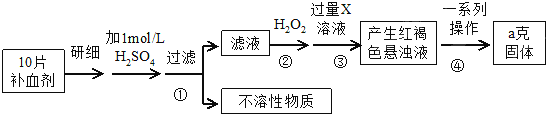
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
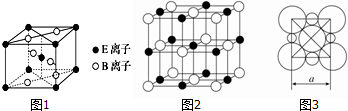
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaOH | B. | NH3•H2O | C. | ZnO | D. | ZnCl2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ${\;}_{77}^{192}$Ir和${\;}_{77}^{193}$Ir是兩種核素 | |
| B. | ${\;}_{77}^{192}$Ir和${\;}_{77}^{193}$Ir是兩種元素 | |
| C. | Ir是主族元素 | |
| D. | 由${\;}_{77}^{193}$Ir經過中子輻射后獲得${\;}_{77}^{192}$Ir是化學變化 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com