
| 實驗操作與現象 | 實驗結論 | |
| 步驟一 | 將該固體全部溶于于得無色溶液; | 肯定無Cu2+. |
| 步驟二 | 向上述溶液中加入足量鹽酸,產生無色無味的氣體共收集到2.24L(標準狀況); | 肯定有CO32- 肯定無Ba2+ |
| 步驟三 | 向步驟二所得溶液中繼續加入足量BaCl2溶液,產生沉淀,過濾并洗滌干燥后得46.6g白色沉淀. | 肯定有SO42- |
| 步驟四 | 向步驟三所得濾液中加入AgNO3溶液,得白色沉淀. |
分析 步驟一中得到無色溶液,一定不含Cu2+;
步驟二中加入足量鹽酸,產生無色無味的氣體共收集到2.24L(標準狀況),氣體為CO2,一定含CO32-,且n(CO32-)=$\frac{2.24L}{22.4L/mol}$=0.1mol;由離子之間不能結合生成沉淀可知,一定不含Ba2+;
步驟三中繼續加入足量BaCl2溶液,產生沉淀,過濾并洗滌干燥后得46.6g白色沉淀,白色沉淀為硫酸鋇,一定含SO42-,n(SO42-)=$\frac{46.6g}{233g/mol}$=0.2mol;
步驟四中,白色沉淀為AgCl,但步驟二、三中引入氯離子,不能確定原溶液中是否含Cl-,然后結合電荷守恒來解答.
解答 解:步驟一中得到無色溶液,一定不含Cu2+;
步驟二中加入足量鹽酸,產生無色無味的氣體共收集到2.24L(標準狀況),氣體為CO2,一定含CO32-,且n(CO32-)=$\frac{2.24L}{22.4L/mol}$=0.1mol;由離子之間不能結合生成沉淀可知,一定不含Ba2+;
步驟三中繼續加入足量BaCl2溶液,產生沉淀,過濾并洗滌干燥后得46.6g白色沉淀,白色沉淀為硫酸鋇,一定含SO42-,n(SO42-)=$\frac{46.6g}{233g/mol}$=0.2mol;
步驟四中,白色沉淀為AgCl,但步驟二、三中引入氯離子,不能確定原溶液中是否含Cl-,
故答案為:
| 實驗操作與現象 | 實驗結論 | |
| 步驟一 | 將該固體全部溶于于得無色溶液; | 肯定無Cu2+ |
| 步驟二 | 向上述溶液中加入足量鹽酸,產生無色無味的氣體共收集到2.24L(標準狀況); | 肯定有CO32-, 肯定無Ba2+ |
| 步驟三 | 向步驟二所得溶液中繼續加入足量BaCl2溶液,產生沉淀,過濾并洗滌干燥后得46.6g白色沉淀. | 肯定有SO42- |
| 步驟四 | 向步驟三所得濾液中加入AgNO3溶液,得白色沉淀. |
點評 本題考查無機物的推斷,把握常見離子的檢驗方法、離子反應及電荷守恒為解答的關鍵,側重分析與推斷、應用能力的考查,題目難度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 氣體甲可與Z的某種氫化物反應生成強酸 | |
| B. | 化合物乙中一定只有共價鍵 | |
| C. | W元素的某種單質可在電子工業用于生產半導體材料 | |
| D. | X分別與Y、Z、M、W形成的常見化合物中,穩定性最好的是XM |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
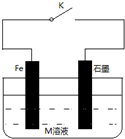
| A. | 常溫下,關閉K時,若M溶液為濃硫酸,則石墨上有氫氣放出 | |
| B. | 關閉K時,若M為氯化鈉,則鐵電極的電極反應式為:O2+4e-+2H2O═4OH- | |
| C. | 關閉K時,若M為則硫酸銨,則石墨極的電極反應式為:2H++2e-═H2↑ | |
| D. | 關閉K時,若M溶液為海水,石墨換成銅或銀,則稱為外加電流的陰極保護法 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | -824.39 kJ•mol-1 | B. | +627.6 kJ•mol-1 | ||
| C. | -744.7 kJ•mol-1 | D. | -169.4 kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 丙烷、丁烷、正戊烷的沸點依次降低 | |
| B. | 乙二醇、丙氨酸均可發生縮聚反應 | |
| C. | 蔗糖和麥芽糖水解的最終產物都是葡萄糖 | |
| D. | 飽和(NH4)2SO4溶液可導致蛋清液變性凝固 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 常溫下,向100mL 0.l mol.L-lHCl的溶液p 中逐滴加入0.2mol.L-lMOH溶液的過程中,其pH變化如圖所示(溶液體積變化忽略不計).下列說法中正確的是( )
常溫下,向100mL 0.l mol.L-lHCl的溶液p 中逐滴加入0.2mol.L-lMOH溶液的過程中,其pH變化如圖所示(溶液體積變化忽略不計).下列說法中正確的是( )| A. | MOH為一元強堿 | |
| B. | N點水的電離程度小于K點水的電離程度 | |
| C. | 在K點,c(M+)>c(Cl-)>c(OH-)>c(H+) | |
| D. | K點對應的溶液中,有c( MOH)+c( M+)=0.2 mol.L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 自然界存在豐富的碳、氮、硅、磷、鐵等元素,它們可形成單質及許多化合物.按要求回答下列問題:
自然界存在豐富的碳、氮、硅、磷、鐵等元素,它們可形成單質及許多化合物.按要求回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com